题目内容
5.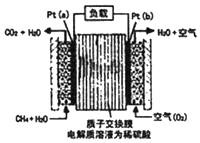 某种甲烷燃料电池采用铂作电极,电池中的质子交换膜只允许质子和水分子通过,其基本结构如图,电池总反应为:CH4+2O2═CO2+2H2O.下列有关说法正确的是( )
某种甲烷燃料电池采用铂作电极,电池中的质子交换膜只允许质子和水分子通过,其基本结构如图,电池总反应为:CH4+2O2═CO2+2H2O.下列有关说法正确的是( )| A. | 电子由a极流出经过负载流向b极 | |
| B. | 电解质溶液中H+移向a极 | |
| C. | 每转移1mole-,消耗1.6gCH4 | |
| D. | b极上的电极反应式为:O2+2H2O+4e-=4OH- |
分析 该燃料电池中,通入燃料的电极为负极,所以a 是负极,负极上失电子发生氧化反应,电极反应式为CH4+2H2O-8e-═CO2+8H+,通入氧化剂的电极为正极,所以b 是正极,正极上得电子发生还原反应,电极反应式为O2+4H++4e-═2H2O,由此分析解答.
解答 解:A.通入燃料的电极为负极,所以a 是负极,通入氧化剂的电极为正极,所以b 是正极,则电子由a极流出经过负载流向b极,故A正确;
B.b 是正极,电解质溶液中H+移向b极,故B错误;
C.a 是负极,电极反应式为CH4+2H2O-8e-═CO2+8H+,所以每转移1mole-,消耗2gCH4,故C错误;
D.b 是正极,正极上得电子发生还原反应,电极反应式为O2+4H++4e-═2H2O,故D错误;
故选A.
点评 本题考查了燃料电池,根据电解质溶液的酸碱性结合正负极上发生的反应来分析解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.丙烯酸可与水反应生成乳酸,化学方程式如下,下列说法正确的是( )
CH2=CH-COOH+H2O$\stackrel{一定条件}{→}$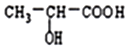
CH2=CH-COOH+H2O$\stackrel{一定条件}{→}$

| A. | 该反应为加成反应,没有副产物生成 | |
| B. | 可用Br2/CCl4溶液鉴别丙烯酸和乳酸 | |
| C. | 丙烯酸与乳酸都属于有机酸,两者不发生反应 | |
| D. | 1mol乳酸分别与足量Na、NaOH、NaHCO3反应,消耗三者物质的量之比为2:2:1 |
20.25℃时,向10mL0.1mol/L H2A溶液中滴加等浓度的NaOH溶液,混合后溶液的pH 与所加NaOH 溶液的体积关系如图所示.下列叙述正确的是( )

| A. | NaHA的电离方程式为NaHA?Na++HA- | B. | B点:c(H2A)+c(H+)=c(OH-)+c(A2-) | ||
| C. | C点:c(Na+)=c(A2-)+c(HA-) | D. | D点:c(Na+)>c(A2-)>c(HA-)>c(OH-)>c(H+) |
10.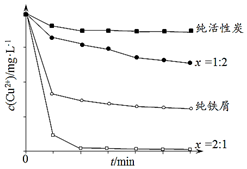 工业上常用铁碳混合物处理含Cu2+废水获得金属铜.当保持铁屑和活性炭总质量不变时,测得废水中Cu2+浓度在不同铁碳质量比(x)条件下随时间变化的曲线如图所示.下列推论不合理的是( )
工业上常用铁碳混合物处理含Cu2+废水获得金属铜.当保持铁屑和活性炭总质量不变时,测得废水中Cu2+浓度在不同铁碳质量比(x)条件下随时间变化的曲线如图所示.下列推论不合理的是( )
 工业上常用铁碳混合物处理含Cu2+废水获得金属铜.当保持铁屑和活性炭总质量不变时,测得废水中Cu2+浓度在不同铁碳质量比(x)条件下随时间变化的曲线如图所示.下列推论不合理的是( )
工业上常用铁碳混合物处理含Cu2+废水获得金属铜.当保持铁屑和活性炭总质量不变时,测得废水中Cu2+浓度在不同铁碳质量比(x)条件下随时间变化的曲线如图所示.下列推论不合理的是( )| A. | 活性炭对Cu2+具有一定的吸附作用 | |
| B. | 铁屑和活性炭会在溶液中形成微电池,铁为负极 | |
| C. | 增大铁碳混合物中铁碳比(x),一定会提高废水中Cu2+的去除速率 | |
| D. | 利用铁碳混合物回收含Cu2+废水中铜的反应原理:Fe+Cu2+═Fe2++Cu |
14.在含有大量H+、Ca2+、Cl-溶液中,还可以大量共存的离子是( )
| A. | OH- | B. | CO32- | C. | Ag+ | D. | Mg2+ |
16.下列有关仪器的名称、图形、操作的叙述均正确的是( )
| 选项 | A | B | C | D |
| 名称 | 250mL容量瓶 | 分液漏斗 | 酸式滴定管 | 冷凝管 |
| 图形 |  |  |  | 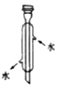 |
| 操作 | 定容时仰视刻度, 则配得的溶液浓 度偏小 | 用酒精萃取水中 碘从上倒出 | 可用于量取 Na2CO3溶液 | 蒸馏实验中将 蒸气冷凝为液体 |
| A. | A | B. | B | C. | C | D. | D |
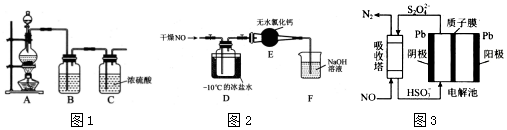
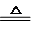 MnCl2+Cl2↑+H2O.装置B中盛放的试剂为饱和食盐水,其作用为除去氯气中的氯化氢气体.
MnCl2+Cl2↑+H2O.装置B中盛放的试剂为饱和食盐水,其作用为除去氯气中的氯化氢气体. .
.