题目内容
17.下列物质的性质和用途对应正确的是( )| A. | 用石英砂制太阳能电池 | |
| B. | 高温下用铝热法炼铁制备钢材 | |
| C. | 液氨汽化时吸收大量的热,可用作制冷剂 | |
| D. | Fe比Cu活泼,可用FeCl3溶液腐蚀线路板上的Cu |
分析 A.石英的主要成分是二氧化硅,太阳能电池的主要成分是硅;
B.用铝热反应冶炼铁成本太高;
C.液氨在挥发时会吸收大量的热;
D.三价铁离子的氧化性大于铜离子.
解答 解:A.石英砂的主要成分是二氧化硅,二氧化硅是光导纤维的主要成分,太阳能电池的主要成分是硅,故A错误;
B.工业上用电解氧化铝的方法冶炼铝,如果用铝热反应冶炼铁,则导致成本较高,工业上利用碳还原铁矿石来制备铁,故B错误;
C.C.液氨在挥发时会吸收大量的热,导致周围的温度降低,所以液氨可以作制冷剂,故C正确;
D.三价铁离子的氧化性大于铜离子,所以可用FeCl3溶液腐蚀线路板上的Cu,与Fe的活泼性无关,故D错误;
故选C.
点评 本题考查了金属的冶炼、铁离子的性质、硅及其化合物的用途等知识点,明确反应原理、物质的性质是解本题关键,结合化学与工业生产来分析解答,题目难度不大.

练习册系列答案
相关题目
5.已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4+Na2CO3:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
(2)CuSO4+Na2S:Cu2++S2-=CuS↓
下列几种物质的溶解度大小的比较中,正确的是( )
(1)CuSO4+Na2CO3:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
(2)CuSO4+Na2S:Cu2++S2-=CuS↓
下列几种物质的溶解度大小的比较中,正确的是( )
| A. | CuS<Cu(OH)2<CuCO3 | B. | CuCO3<Cu(OH)2<CuS | C. | CuS<CuCO3<Cu(OH)2 | D. | Cu(OH)2<CuCO3<CuS |
12.向某溶液中滴加过量盐酸,生成能使澄清石灰水变浑浊的无色气体,则有关推断不正确的是( )
| A. | 该气体一定是CO2 | |
| B. | 如果该气体无味,则该溶液中可能含CO32- | |
| C. | 如果该气体无味,则该溶液中可能含CO32-、HCO3-或者两者均有 | |
| D. | 如果该气体具有刺激性气味,则该溶液中可能含SO32-、HSO3-或者两者均有 |
2.下列实验装置能达到实验目的是( )
| A. | 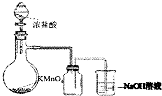 实验室制取并收集Cl2 | B. | 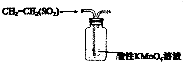 检验乙烯中是否含有SO2 | ||
| C. | 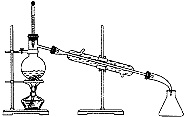 分离Br2和H20的混合物 | D. | 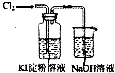 验证氧化性Cl>I2 |
9.下列图示箭头方向表示与某种常见试剂在通常条件下(不含电解)发生转化,其中6步转化均能一步实现的一组物质是( )
| 选项 | W | X | Y | Z | 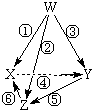 |
| A | N2 | NH3 | NO | NO2 | |
| B | Na | Na2O2 | NaOH | Na2CO3 | |
| C | Cu | CuSO4 | CuCl2 | Cu(OH)2 | |
| D | Al | Al2(SO4)3 | AlCl3 | NaAlO2 |
| A. | N2 NH3 NO NO2 | B. | Na Na2O2 NaOH Na2CO3 | ||
| C. | Cu CuSO4 CuCl2 Cu(OH)2 | D. | Al Al2(SO4)3 AlCl3 NaAlO2 |
6.2006年11月23日中科院网报道,纳米Fe3O4晶体材料可以作为核磁共振造影增强剂,用于疾病的诊断和作为药物载体用于疾病的治疗.其制备过程如图,下列叙述合理 的是( )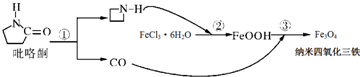

| A. | Fe3O4可以表示为FeO•Fe2O3,属于混合物 | |
| B. | 在反应②中FeCl3•6H2O被环丙胺(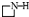 )还原为FeOOH )还原为FeOOH | |
| C. | 纳米四氧化三铁材料为胶体 | |
| D. | 反应③的化学方程式是:6FeOOH+CO═2Fe3O4+3H2O+CO2 |
7.下列有关氧化还原反应的说法正确的是( )
| A. | 一定有电子得失或偏移 | B. | 氧化反应一定先于还原反应 | ||
| C. | 氧化剂发生氧化反应 | D. | 其实质是元素化合价发生变化 |
 .
. 、
、 .
.