题目内容
10.下列关于电池的说法正确的是( )| A. | 原电池负极金属一定比正极金属的金属性活泼 | |
| B. | 原电池中电解质溶液中的阳离子向负极移动 | |
| C. | 碱性锌猛锰干电池的负极反应为:Zn-2e-+4OH-=ZnO22-+2H2O | |
| D. | 铅蓄电池工作时转移电子数为2NA时,负极材料质量减少207g |
分析 A、原电池如果是燃料电池,铂电极惰性电极,两极的金属活泼性相同;
B、原电池中电解质溶液中的阳离子向正极移动;
C、碱性锌猛锰干电池负极发生氧化反应,反应式为Zn+2OH--2e-=Zn(OH)2;
D、根据Pb+SO42--2e-=PbSO4,负极质量增加.
解答 解:A、原电池如果是燃料电池,铂电极惰性电极,两极的金属活泼性相同,所以原电池负极金属不一定比正极金属的金属性活泼,故A错误;
B、原电池中电解质溶液中的阳离子向正极移动,故B错误;
C、负极发生氧化反应,反应式为Zn+2OH--2e-=Zn(OH)2或Zn-2e-+4OH-=ZnO22-+2H2O,故C正确;
D、铅蓄电池工作时转移电子数为2NA时,根据Pb+SO42--2e-=PbSO4,负极质量增加,增加的质量为硫酸根离子的质量,每通过2mol电子负极质量增加96g,故D错误;
故选C.
点评 本题考查学生原电池的电极的构成条件以及工作原理知识,可以根据所学知识来回答,较简单.

练习册系列答案
相关题目
20.将AgCl和AgBr的饱和溶液等体积混合,再加入足量的浓AgNO3溶液,下列说法正确的是( )
| A. | 只有AgBr沉淀生成 | B. | 生成等物质的量的AgCl和AgBr沉淀 | ||
| C. | 沉淀的物质的量:AgCl多于AgBr | D. | 沉淀的物质的量:AgCl少于AgBr |
1.A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X,它们有如图所示的转化关系(部分产物及反应条件已略去).下列推断正确的是( )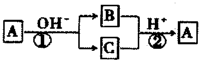

| A. | 反应①和②是可逆反应 | B. | 反应①和②一定为氧化还原反应 | ||
| C. | X元素可能是金属,也可能是非金属 | D. | X元素为铝 |
18.现有4.9gMgO、Mg(OH)2的固体混合物,与l00g9.8%的稀H2SO4恰好完全反应,形成不饱和溶液.则原固体混合物中镁元素的质量为( )
| A. | 1.2g | B. | 1.6g | C. | 2.4g | D. | 4.8g |
5.在密闭的容器中进行某一个可逆反应,由A与B反应生成产物C,反应速率的关系:v(B)=3v(A),3v(C)=2v(B),v(C)=2v(A).则此反应可表示为( )
| A. | A+3B?2C | B. | 2A+2B?3C | C. | 3A+B?C | D. | A+B?C |
15.使用氢氧燃料电池的公共汽车已在北京街头出现.某种以30%KOH溶液为电解质的氢氧燃料电池在使用时的电极反应如下:
2H2+4OH--4e-═4H2O
O2+2H2O+4e-═4OH-.
下列有关该氢氧燃料电池的说法中,正确的是( )
2H2+4OH--4e-═4H2O
O2+2H2O+4e-═4OH-.
下列有关该氢氧燃料电池的说法中,正确的是( )
| A. | H2在正极发生氧化反应 | |
| B. | 供电时的总反应为:2H2+O2═2H2O | |
| C. | 氢氧燃料电池中H2和O2燃烧放出的热量转变为电能 | |
| D. | 氢氧燃料电池不属于环境友好电池 |
2.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中少量的CO | 点燃 |
| B | 除去CuSO4溶液中的少量FeSO4 | 加入足量的铜粉 |
| C | 鉴别澄清石灰水和NaOH溶液 | 加入稀盐酸 |
| D | 鉴别硬水和软水 | 加入肥皂水 |
| A. | A | B. | B | C. | C | D. | D |
19.合成氨反应N2+3H2$?_{△}^{Fe}$2NH3,其化学反应速率可以用v(H2)、v(N2)、v(NH3)来表示,单位[mol/(L•s)],那么正确的关系式是( )
| A. | v(H2)=v(N2)=v(NH3) | B. | v(H2)=3v(N2) | C. | v(NH3)=1.5v(H2) | D. | v(N2)=2v(H2) |