题目内容
同一主族的两种元素的原子序数之差不可能是( )
| A、16 | B、26 | C、46 | D、36 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:相邻两个周期同主族元素的原子序数相差2、8、18、32,以此判断.
解答:
解:A.如0族中第一周期与第三周期元素相差16,故A不选;
B.如ⅣA等第二周期与第四周期元素相差26,故B不选;
C.2、8、18、32的组合不能得到46,则同主族原子序数之差不可能是46,故C选;
D.如零族等第三周期与第五周期元素相差36,故D不选;
故选C.
B.如ⅣA等第二周期与第四周期元素相差26,故B不选;
C.2、8、18、32的组合不能得到46,则同主族原子序数之差不可能是46,故C选;
D.如零族等第三周期与第五周期元素相差36,故D不选;
故选C.
点评:本题考查元素周期表的结构及应用,为高频考点,把握元素的位置、周期中的元素种类数为解答的关键,注意利用列举法,题目难度不大.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
某化合物6.4g在氧气中完全燃烧,只生成8.8g CO2和7.2g H2O.下列说法正确的是( )
| A、该化合物仅含碳、氢两种元素 |
| B、该化合物中碳、氢原子个数比为1:4 |
| C、无法确定该化合物是否含有氧元素 |
| D、该化合物一定是C2H8O2 |
有机物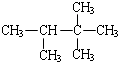 的名称是( )
的名称是( )
 的名称是( )
的名称是( )| A、2,3,3-三甲基丁烷 |
| B、2,3-三甲基丁烷 |
| C、2,2,3-三甲基丁烷 |
| D、2,3-三甲基丁烷 |
设NA表示阿伏加德罗常数,则下列说法中正确的是( )
| A、22.4L O2含有的O2分子个数为NA | ||
| B、在标准状况下,4.48L H2O中所含的原子总数为0.6NA | ||
C、一个氧原子的质量为
| ||
| D、常温常压下,22g CO2含有的原子个数为1.5NA |
反应2SO2+O2
2SO3经一段时间后,SO3的浓度增加了0.8mol?L-1,在这段时间内用O2表示的反应速率为0.04mol?L-1?s-1,则这段时间为( )
| ||
| △ |
| A、0.1s | B、2.5s |
| C、5s | D、10s |
 如图为PCl5(g)?PCl3(g)+Cl2(g)(正反应为吸热反应),从平衡状态Ⅰ移动到平衡状态Ⅱ的反应速率(v)与时间(t)的曲线,此图表示的变化是( )
如图为PCl5(g)?PCl3(g)+Cl2(g)(正反应为吸热反应),从平衡状态Ⅰ移动到平衡状态Ⅱ的反应速率(v)与时间(t)的曲线,此图表示的变化是( )| A、降温 |
| B、降压 |
| C、增加PCl5的量 |
| D、增加PCl3的量 |
对已经达到化学平衡的下列反应:X(g)+2Y(g)?Z(g)△H>0,当改变条件时,对反应产生的影响描述正确的是( )
| A、减小压强(通过改变容积体积)时,正反应速率减小,逆反应速变增大,平衡向逆反应方向移动 |
| B、增大压强(通过改变容积体积)时,Z的物质的量浓度增大,X、Y的物质的量浓度减小 |
| C、升高温度时,正、逆反应速率都增大,平衡向正反应方向移动 |
| D、容积体积不变,再通入一定量的X,平衡正向移动,Z的物质的量分数一定增大 |
下列各物质或其主要成分的名称(或俗名)、化学式、类别一致的是( )
| A、胆矾 CuSO4?5H2O 混合物 |
| B、氖气 Ne 单质 |
| C、烧碱 NaOH 氧化物 |
| D、纯碱 NaOH 碱 |



