题目内容
在标准状况下,一个盛满空气的容器重95.3g(已知空气的平均相对分子质量为29.0),在相同条件下若改盛满SO2气体时重98.8g,则此容器的体积约是( )
| A、0.560L |
| B、1.12L |
| C、2.24L |
| D、3.36L |
考点:物质的量的相关计算
专题:计算题
分析:在标准状况下,盛满空气和改盛满SO2气体的体积相等,等于容器的体积,则空气和SO2的物质的量相等,假设气体的物质的量为n,进而根据V=nVm可计算此容器的体积.
解答:
解:假设气体的物质的量为nmol,容器的质量为mg,则:
联立方程,解得
根据V=nVm则此容器的体积约V=nVm=0.1mol×22.4mol/L=0.224L,
故选C.
|
|
根据V=nVm则此容器的体积约V=nVm=0.1mol×22.4mol/L=0.224L,
故选C.
点评:本题考查了阿伏伽德罗定律及其推论,明确相同条件下相同体积的不同气体的物质的量相等为解答关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
化学平衡状态是( )
| A、静止止状态 |
| B、正反应速率大于逆反应速率 |
| C、不可改变的状态 |
| D、反应物与生成物浓度保持不变的状态 |
把氯气通入紫色石蕊试液中,可以观察到的现象是( )
| A、先变蓝后变红 |
| B、先变红后褪色 |
| C、先变红后变紫 |
| D、先变紫后变红 |
不能用排水收集法收集的气体是( )
| A、氨气 | B、氧气 |
| C、二氧化硫 | D、一氧化氮 |
糖类、油脂和蛋白质都是人体必需的基本营养物质,下列说法中不正确的是( )
| A、淀粉、油脂和蛋白质都能发生水解反应 |
| B、糖类、油脂和蛋白质都属于高分子化合物 |
| C、氨基酸既可以与盐酸反应,也能与NaOH反应 |
| D、采用多次盐析和溶解,可以分离提纯蛋白质 |
实验室在配制Fe2(SO4)3水溶液时,先把Fe2(SO4)3晶体溶解在较浓H2SO4中,再加水稀释至所需浓度,如此操作的目的是( )
| A、防止硫酸铁分解 |
| B、抑制Fe2(SO4)3水解 |
| C、提高硫酸铁的溶解度 |
| D、提高溶液的pH |
已知2SO2+O2?2SO3为放热反应,对该反应的下列说法正确的是( )
| A、O2的能量一定高于SO2的能量 |
| B、2molSO2和1molO2的总能量一定高于2molSO3的总能量 |
| C、SO2的能量一定高于SO3的能量 |
| D、因该反应为放热反应,故不必加热就可发生 |
短周期元素W、X、Y、Z的原子序数依次增大,W与Y,X与Z分别位于同一主族,W与X可形成两种常见气体WX2和WX,Y原子的内层电子总数是其最外层电子数的2.5倍,下列叙述中不正确的是( )
| A、WX2分子中所有原子最外层都已满足8电子结构 |
| B、WX2、ZX2的化学键类型相同 |
| C、原子半径大小顺序为:X<W<Y<Z |
| D、乙醇、乙酸、葡萄糖、油脂中均含W、X两种元素 |
下列实验操作或装置符合实验要求的是( )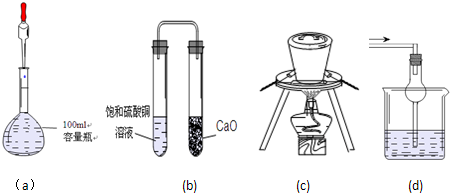

| A、(a) 可用于定容并量取15.00 mL NaOH溶液 |
| B、(b)装置放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
| C、(c)可用于高温煅烧石灰石 |
| D、(d)可用于易溶于水的尾气吸收 |