题目内容
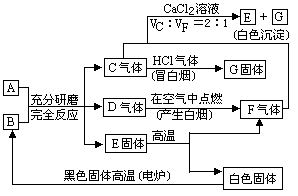
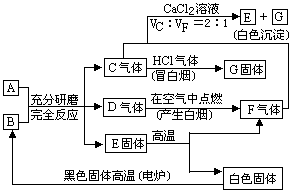
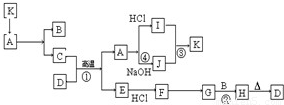
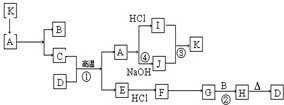 如图每一方框表示有关反应的某一反应物或生成物,有关操作已略去.又知A为高熔点物质,可做耐火材料,A在一定条件下可生成B和C,B为无色气体,D为一种天然出产的矿石的主要成分,可作为颜料.
如图每一方框表示有关反应的某一反应物或生成物,有关操作已略去.又知A为高熔点物质,可做耐火材料,A在一定条件下可生成B和C,B为无色气体,D为一种天然出产的矿石的主要成分,可作为颜料.
试回答:
(1)写出化学式:A______,D______.
(2)写出化学方程式:反应①______.反应②______.
(3)写出离子方程式:③:______.④:______.
解:A为高熔点物质,可做耐火材料,为Al2O3,电解可生成O2和Al,则B为O2,C为Al,C和D在高温下发生反应,应为铝热反应,则D为赤铁矿中的Fe2O3,I为AlCl3,J为NaAlO2,K为Al(OH)3,E为Fe,F为FeCl2,G为Fe(OH)2,H为Fe(OH)3,则
(1)由以上分析可知A为Al2O3,D为Fe2O3,故答案为:Al2O3;Fe2O3;
(2)反应①为Al和Fe2O3的铝热反应,方程式为2Al+Fe2O3 2Fe+Al2O3,
2Fe+Al2O3,
反应②为Fe(OH)2被氧化为Fe(OH)3的反应,方程式为4Fe(OH)2+O2+H2O=4Fe(OH)3,
故答案为:2Al+Fe2O3 2Fe+Al2O3;4Fe(OH)2+O2+H2O=4Fe(OH)3;
2Fe+Al2O3;4Fe(OH)2+O2+H2O=4Fe(OH)3;
(3)Al3+与AlO2-发生互促水解生成Al(OH)3,反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓,
Al2O3为两性氧化物,与碱反应的离子方程式为Al2O3+2OH-═2AlO2-+H2O,
故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓;Al2O3+2OH-═2AlO2-+H2O.
分析:由题给有关物质的某些性质等,可判断A为两性氧化物Al2O3,电解可生成O2和Al,则B为O2,C为Al,C和D在高温下发生反应,应为铝热反应,则D为赤铁矿中的Fe2O3,I为AlCl3,J为NaAlO2,K为Al(OH)3,E为Fe,F为FeCl2,G为Fe(OH)2,H为Fe(OH)3,结合相关物质的性质可解答该题.
点评:本题考查无机物的推断,题目难度中等,明确物质的种类为解答该题的关键,本题注意把握物质的特性、用途以及在地壳中的存在,常作为推断题的突破口,学习中注意积累和体会.
(1)由以上分析可知A为Al2O3,D为Fe2O3,故答案为:Al2O3;Fe2O3;
(2)反应①为Al和Fe2O3的铝热反应,方程式为2Al+Fe2O3
 2Fe+Al2O3,
2Fe+Al2O3,反应②为Fe(OH)2被氧化为Fe(OH)3的反应,方程式为4Fe(OH)2+O2+H2O=4Fe(OH)3,
故答案为:2Al+Fe2O3
 2Fe+Al2O3;4Fe(OH)2+O2+H2O=4Fe(OH)3;
2Fe+Al2O3;4Fe(OH)2+O2+H2O=4Fe(OH)3;(3)Al3+与AlO2-发生互促水解生成Al(OH)3,反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓,
Al2O3为两性氧化物,与碱反应的离子方程式为Al2O3+2OH-═2AlO2-+H2O,
故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓;Al2O3+2OH-═2AlO2-+H2O.
分析:由题给有关物质的某些性质等,可判断A为两性氧化物Al2O3,电解可生成O2和Al,则B为O2,C为Al,C和D在高温下发生反应,应为铝热反应,则D为赤铁矿中的Fe2O3,I为AlCl3,J为NaAlO2,K为Al(OH)3,E为Fe,F为FeCl2,G为Fe(OH)2,H为Fe(OH)3,结合相关物质的性质可解答该题.
点评:本题考查无机物的推断,题目难度中等,明确物质的种类为解答该题的关键,本题注意把握物质的特性、用途以及在地壳中的存在,常作为推断题的突破口,学习中注意积累和体会.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
| |||||||||||||||
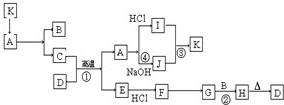 如图每一方框表示有关反应的某一反应物或生成物,有关操作已略去.又知A为高熔点物质,可做耐火材料,A在一定条件下可生成B和C,B为无色气体,D为一种天然出产的矿石的主要成分,可作为颜料.
如图每一方框表示有关反应的某一反应物或生成物,有关操作已略去.又知A为高熔点物质,可做耐火材料,A在一定条件下可生成B和C,B为无色气体,D为一种天然出产的矿石的主要成分,可作为颜料.