题目内容
X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增.已知X的最外层电子数是次外层电子数的3倍,X、M同主族,Y在同周期主族元素中原子半径最大.Z和N可以形成ZN2型化合物.下列有关说法正确的是( )
| A、单质的氧化性:X<M |
| B、最高价氧化物对应水化物的碱性:Y>Z |
| C、气态氢化物的热稳定性:M>N |
| D、X与Y只能形成一种化合物 |
考点:原子结构与元素的性质
专题:
分析:X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增,X的最外层电子数是次外层电子数的3倍,最外层电子数不超过8个,所以X元素次外层电子数是2,其最外层电子数是6,为O元素;X、M同主族,且M原子序数大于X,所以M为S元素;
N原子序数大于M且为短周期主族元素,所以N是Cl元素;
Y在同周期主族元素中原子半径最大,Y原子序数大于X,所以Y为Na元素;
Z和N可以形成ZN2型化合物,Z原子序数大于11而小于16,所以N为Mg元素,再结合物质结构、性质解答.
N原子序数大于M且为短周期主族元素,所以N是Cl元素;
Y在同周期主族元素中原子半径最大,Y原子序数大于X,所以Y为Na元素;
Z和N可以形成ZN2型化合物,Z原子序数大于11而小于16,所以N为Mg元素,再结合物质结构、性质解答.
解答:
解:X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增,X的最外层电子数是次外层电子数的3倍,最外层电子数不超过8个,所以X元素次外层电子数是2,其最外层电子数是6,为O元素;X、M同主族,且M原子序数大于X,所以M为S元素;
N原子序数大于M且为短周期主族元素,所以N是Cl元素;
Y在同周期主族元素中原子半径最大,Y原子序数大于X,所以Y为Na元素;
Z和N可以形成ZN2型化合物,Z原子序数大于11而小于16,所以N为Mg元素,
A.同一主族元素,元素单质的氧化性随着原子序数增大而减小,原子序数X>M,所以单质的氧化性X>M,故A错误;
B.金属性Y>Z,所以最高价氧化物的水化物碱性Y>Z,故B正确;
C.非金属性越强其气态氢化物越稳定,非金属性M<N,所以气态氢化物的稳定性M<N,故C错误;
D.X是O、Y是Na元素,二者能形成Na2O、Na2O2,故D错误;
故选B.
N原子序数大于M且为短周期主族元素,所以N是Cl元素;
Y在同周期主族元素中原子半径最大,Y原子序数大于X,所以Y为Na元素;
Z和N可以形成ZN2型化合物,Z原子序数大于11而小于16,所以N为Mg元素,
A.同一主族元素,元素单质的氧化性随着原子序数增大而减小,原子序数X>M,所以单质的氧化性X>M,故A错误;
B.金属性Y>Z,所以最高价氧化物的水化物碱性Y>Z,故B正确;
C.非金属性越强其气态氢化物越稳定,非金属性M<N,所以气态氢化物的稳定性M<N,故C错误;
D.X是O、Y是Na元素,二者能形成Na2O、Na2O2,故D错误;
故选B.
点评:本题考查原子结构和元素周期律关系,侧重考查学生灵活运用知识解答问题能力,正确推断元素是解本题关键,熟练掌握元素周期律、物质结构,题目难度不大.

练习册系列答案
相关题目
从海水中提取镁的工业流程如图所示,下列说法正确的是( )

| A、在实验室进行②的操作需用到坩埚、坩埚钳、玻璃棒、酒精灯 |
| B、步骤⑥电解MgCl2时,阴极产生H2 |
| C、步骤⑤应将晶体置于HCl气体氛围中脱水 |
| D、上述工艺流程中的反应未涉及氧化还原反应 |
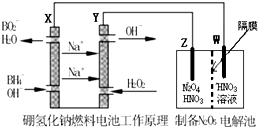 N2O5是一种新型绿色硝化剂,一种制备方法是用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5.工作原理如图:(隔膜不允许水分子通过,H+可以通过)下列说法正确的是( )
N2O5是一种新型绿色硝化剂,一种制备方法是用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5.工作原理如图:(隔膜不允许水分子通过,H+可以通过)下列说法正确的是( )| A、Y是负极,电极反应式:H2O2+2e-=2OH- |
| B、Z是阳极,电极反应式为:N2O4+2HNO3-2e-=2N2O5+2H+ |
| C、电流从X流出经导线流入W极 |
| D、制备10.8gN2O5至少需要消耗硼氢化钠0.87g |
已知反应:①101kPa时,2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol
又知由H2和O2两种气体反应生成1mol液态水比生成1mol气态水多放出44kJ热量.下列结论中正确的是( )
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol
又知由H2和O2两种气体反应生成1mol液态水比生成1mol气态水多放出44kJ热量.下列结论中正确的是( )
| A、H2的燃烧热为285.8 kJ/mol | ||
B、H2和O2反应生成液态水时的热化学方程式为H2(g)+
| ||
| C、稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ | ||
| D、稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
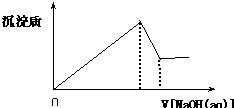 向某溶液中逐滴加入0.5mol/L的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示,则该溶液中可能存在的离子是( )
向某溶液中逐滴加入0.5mol/L的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示,则该溶液中可能存在的离子是( )| A、只有Mg2+ |
| B、只有Al3+ |
| C、有H+、Mg2+和Al3+ |
| D、有Mg2+和Al3+ |
下列各项是关于玻璃棒在若干实验中的用途及操作,其中错误的是( )
①溶解物质时搅拌
②蒸发操作时搅拌液体防止飞溅
③过滤时用玻璃棒引流,其下端在漏斗内滤纸的任意部位
④配制一定体积的物质的量浓度的溶液用玻璃棒引流.
①溶解物质时搅拌
②蒸发操作时搅拌液体防止飞溅
③过滤时用玻璃棒引流,其下端在漏斗内滤纸的任意部位
④配制一定体积的物质的量浓度的溶液用玻璃棒引流.
| A、①③ | B、①② |
| C、只有③ | D、全部错误 |
下列化学用语表示不正确的是( )
A、Na+的结构示意图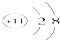 |
B、四氯化碳的电子式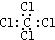 |
| C、二氧化碳的结构式为O=C=O |
| D、乙烯的实验式为 CH2 |
反应mA(g)+nB(g)?pC(g)中,若VA=a mol/(L?s),则VC为( )
A、
| ||
B、
| ||
C、
| ||
D、
|