题目内容
15.汽车尾气处理装置中发生如下反应,2NO+2CO═N2+2CO2,下列说法正确的是( )| A. | NO是氧化剂 | B. | CO发生还原反应 | ||
| C. | NO失去电子 | D. | 该反应是复分解反应 |
分析 2NO+2CO═N2+2CO2中,C元素的化合价升高,则CO为还原剂,N元素的化合价降低,则NO为氧化剂,结合氧化还原反应基本概念解答.
解答 解:A.NO中N元素的化合价降低,被还原,则NO为氧化剂,故A正确;
B.C元素的化合价升高,CO为还原剂,发生氧化反应,故B错误;
C.NO中N元素的化合价降低,得电子,故C错误;
D.该反应是氧化还原反应,不是复分解反应,故D错误;
故选A.
点评 本题考查氧化还原反应,把握氧化还原反应中元素的化合价变化为解答的关键,注意从化合价角度分析,侧重基本概念的考查,题目难度不大.

 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案| A. | Fe3O4是还原剂 | B. | CO是氧化剂 | ||
| C. | 1mol Fe3O4得到6mol电子 | D. | 4molCO失去8mol电子 |
①不溶于水的盐(CaCO3、BaSO4等)都是电解质
②酸、碱、盐都是强电解质
③0.5mol•L-1 所有一元酸中氢离子浓度都是0.5mol•L-1
④电解质在通电情况下才能发生电离
⑤电解质溶液导电的原因是在溶液中有自由移动的阴阳离子
⑥熔融的电解质都能导电.
| A. | ①③⑤⑥ | B. | ②④⑤⑥ | C. | 只有⑤ | D. | 只有⑤⑥ |
| A. | 小苏打--Na2CO3 | B. | 生石灰--Ca (OH)2 | C. | 甲醛--CH3OH | D. | 烧碱--NaOH |
| A. | 可以用四氯化碳把溴水中的溴萃取出来,振荡静置分层后,下层液体为无色 | |
| B. | 萃取分液时,从分液漏斗下口流完下层液体,及时关闭.再打开流出上层液体 | |
| C. | 碘易溶于酒精,微溶于水,故可以用酒精萃取碘水中的碘 | |
| D. | 萃取之后,一般通过分液漏斗将互不相溶的液体分离 |
| A. | Na+、Mg2+、Cl-、SO42- | B. | Mg2+、Ca2+、HCO3-、Cl- | ||
| C. | Ba2+、Al3+、Cl-、NO3- | D. | K+、Cu2+、Cl-、SO42- |
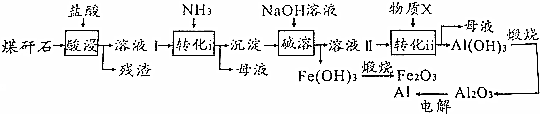
X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。据此回答下列问题:
(1)L的常见原子组成符号为 ;M在元素周期表中的位置为 ;五种元素的原子半径从大到小的顺序是 (用具体元素符号表示)。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为 ,B的结构式为 。Z和L也能组成原子数目比2∶4的分子C, 已知1 mol 液态C和液态B燃烧时生成无毒无害物质,并释放524.5 kJ的热量,试写出该反应的热化学方程式为 。
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为 ,其最高价氧化物对应的水化物化学式为 。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是 (填字母代号)。
A.+99.7 kJ·mol-1 | B.+29.7 kJ·mol-1 | C.-20.6 kJ·mol-1 | D.-241.8 kJ·mol-1 |
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R。写出阳极生成R的电极反应式: 。
 .
. 2,2二甲基丁烷.
2,2二甲基丁烷.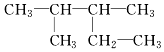 2,3二甲基戊烷.
2,3二甲基戊烷.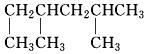 2,4二甲基己烷.
2,4二甲基己烷.