题目内容
10.关于如图所示装置的叙述,正确的是( )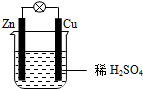
| A. | Cu为负极,Zn为正极 | B. | 电子从铜片经外电路流向锌片 | ||
| C. | 负极反应为:Zn-2e-═Zn2+ | D. | 该装置将电能转化为化学能 |
分析 该装置是将化学能转变为电能的装置,属于原电池,较活泼的金属锌作负极,不活泼的金属铜作正极,负极上锌失电子发生氧化反应,正极上氢离子得电子发生还原反应.
解答 解:A.该原电池中,较活泼的金属锌作负极,较不活泼的金属铜作正极,故A错误;
B.电子从负极流出,即电子从锌流出,经外电路流向正极铜片,故B错误;
C.负极上失电子发生氧化反应,电极反应式为Zn-2e-═Zn2+,故C正确;
D.该装置是将化学能转变为电能的装置,属于原电池,故D错误.
故选C.
点评 本题考查了原电池原理,一般可以根据金属的活泼性确定原电池的正负极,正负极的反应要结合氧化还原反应来分析,题目比较简单.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
1.下列有关环境问题的说法正确的是( )
| A. | 臭氧的体积分数超过10-4%的空气有利于人体健康 | |
| B. | pH在5.6~7.0之间的雨水通常称为酸雨 | |
| C. | 燃煤时加入适量石灰石,可减少废气中SO2的量 | |
| D. | 含磷合成洗涤剂易于被细菌分解,故不会导致水体污染 |
18.对C、N、O元素的有关比较表述不正确的是( )
| A. | 氢化物稳定性:CH4<NH3<H2O | B. | 第一电离能:C<N<O | ||
| C. | 电负性:C<N<O | D. | 氢化物沸点:CH4<NH3<H2O |
5.下列离子方程式正确的是( )
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ | |
| C. | 碳酸钙与稀盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| D. | 向FeCl3溶液中加入氨水:Fe3++3NH3•H2O═Fe(OH)3↓+3NH4+ |
15.下列有关几种常见的金属和非金属及其化合物的说法正确的是( )
| A. | Na、Mg、Al、Fe、Cu都能导电,它们的氧化物都能与酸反应 | |
| B. | 铝热反应是指铝能将所有的金属从其氧化物中置换出来 | |
| C. | CO2、NO、SO2都是非金属氧化物,都属于酸性氧化物 | |
| D. | CaCO3+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸 |
2.在一个固定容积的密闭容器中发生可逆反应:mA(g)+nB(g)?pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,不能说明达到平衡状态的标志是( )
| A. | C的质最不再改变 | |
| B. | 物质的最浓度c(A):c(B):c(C):c(D)=m:n:p:q | |
| C. | 各组分浓度不再改变 | |
| D. | 单位时间内m molA断键,同时pmolC也断键 |
19.某同学用中和滴定的方法测定混有少量Na2CO3的NaOH固体中NaOH的含量,准确称取2.0g样品配制成200mL溶液,然后分三次各取20.00mL溶液于三个洁净的锥形瓶中,分别加入过量BaCl2溶液和1~2滴指示剂,用浓度为0.2000mol•L-1的盐酸标准液进行滴定.
(1)滴定时应选用酚酞作指示剂;到达滴定终点的实验现象是最后一滴盐酸滴入后,溶液由浅红色变为无色且30秒不改变.
(2)下列操作会导致烧碱样品中NaOH含量测定值偏高的是BC.
A.锥形瓶未用待测液润洗
B.酸式滴定管未用标准液润洗
C.在滴定前有气泡,滴定后气泡消失
D.滴定前平视读数,滴定结束俯视读数
E.滴定终点前加水清洗锥形瓶
F.指示剂变色后立即读数
(3)实验相关数据记录如下:
依据表中数据,计算样品中NaOH的质量分数80%.
(1)滴定时应选用酚酞作指示剂;到达滴定终点的实验现象是最后一滴盐酸滴入后,溶液由浅红色变为无色且30秒不改变.
(2)下列操作会导致烧碱样品中NaOH含量测定值偏高的是BC.
A.锥形瓶未用待测液润洗
B.酸式滴定管未用标准液润洗
C.在滴定前有气泡,滴定后气泡消失
D.滴定前平视读数,滴定结束俯视读数
E.滴定终点前加水清洗锥形瓶
F.指示剂变色后立即读数
(3)实验相关数据记录如下:
| 实验编号 | V(烧碱溶液)/mL | V(HCl)/mL | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.60 | 20.62 |
| 2 | 20.00 | 0.80 | 20.78 |
| 3 | 20.00 | 0.20 | 20.90 |
20.用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 等质量的N2和CO所含分子数均为NA | |
| B. | 在标准状况下,22.4L CH4与18g H2O所含的电子数均为10NA | |
| C. | 一定温度下,1L 1mol•L-1的CH3COONa溶液含NA个CH3COO- | |
| D. | 1mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子 |