题目内容
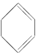
6.如图所示可逆反应在使用和未使用催化剂时,反应过程和能量的对应关系.下列说法正确的是( )
| A. | 反应物的总能量大于生成物的总能量 | |
| B. | 反应产生的热效应Q=E1-E2 | |
| C. | a与b相比,反应的平衡常数一定不同 | |
| D. | a与b相比,a的反应速率更快 |
分析 由图可知,反应物总能量大于生成物总能量,焓变为正逆反应的活化能之差,b为使用催化剂,降低反应的活化能,但焓变不变,以此来解答.
解答 解:A.为放热反应,反应物的总能量大于生成物的总能量,故A正确;
B.焓变为正逆反应的活化能之差,但反应产生的热效应Q=E2-E1,故B错误;
C.b为使用催化剂,平衡常数与温度有关,则a与b相比,反应的平衡常数相同,故C错误;
D.b为使用催化剂,a与b相比,b的反应速率更快,故D错误;
故选A.
点评 本题考查反应热与焓变,为高频考点,把握图中的能量变化、焓变与Q的区别、平衡常数与温度的关系为解答的关键,侧重分析与应用能力的考查,注意催化剂可降低反应的活化能,题目难度不大.

练习册系列答案
相关题目
16.有机物的种类繁多,但其命名是有规则的.下列有机物命名正确的是( )
| A. | 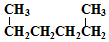 1,4-二甲基丁烷 1,4-二甲基丁烷 | B. | 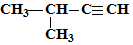 2-甲基-3-丁炔 2-甲基-3-丁炔 | ||
| C. |  2-丁醇 2-丁醇 | D. | CH2Cl-CH2Cl 二氯乙烷 |
14.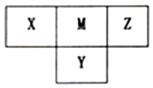 短周期元素X、Y、Z、M在周期表中所处的位置如图所示,四种元素原子的质子数之和为36.下列说法不正确的是( )
短周期元素X、Y、Z、M在周期表中所处的位置如图所示,四种元素原子的质子数之和为36.下列说法不正确的是( )
 短周期元素X、Y、Z、M在周期表中所处的位置如图所示,四种元素原子的质子数之和为36.下列说法不正确的是( )
短周期元素X、Y、Z、M在周期表中所处的位置如图所示,四种元素原子的质子数之和为36.下列说法不正确的是( )| A. | X与Z形成的三原子分子的电子式为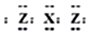 | |
| B. | 简单氢化物稳定性Z>M>Y | |
| C. | X、Y、M分别与Z可形成多种二元共价化合物 | |
| D. | 最高价氧化物的水化物的酸性M>Y>X |
1.X、Y、Z、W为四种短周期主族元素,且原子序数依次递增,其中X、Z同主族,Y原子半径是短周期主族元素中最大的,X原子最外层电子数是核外电子层数的3倍,下列说法正确的是( )
| A. | 原子半径:rW>rZ>rY>rX | |
| B. | Z的氢化物比X的氢化物稳定 | |
| C. | X、Y、Z三种元素组成的化合物不止2种 | |
| D. | W元素氧化物对应水化物的酸性一定强于Z |
11.有关碱金属元素,下列说法正确的是( )
| A. | 单质沸点随原子序数的递增而升高 | |
| B. | 周期表第一列是第ⅠA 族元素,又称碱金属元素 | |
| C. | 金属锂常用于制造锂电池,这跟它还原性强、密度小有关 | |
| D. | 金属锂在空气中燃烧,产物是 Li2O2 |
6.据有关资料显示,在独居石(一种共生矿,化学成分为Ce、La、Nb…的磷酸盐)中,查明有尚未命名的116,124,126号元素.试判断116号元素应位于周期表中的( )
| A. | 第6周期,第ⅣA族 | B. | 第7周期,第ⅥA族 | C. | 第7周期,第ⅣA族 | D. | 第8周期,第ⅥA族 |
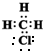 ,
,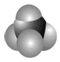 是甲烷的比例模型
是甲烷的比例模型 、
、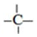 四种基团,若要使烷烃碳个数最少,写出符号条件所有烷烃的结构简式CH3CH2CH(CH3)C(CH3)3、CH3CH(CH3)C(CH3)2CH2CH3、CH3C(CH3)2CH2CH(CH3)2
四种基团,若要使烷烃碳个数最少,写出符号条件所有烷烃的结构简式CH3CH2CH(CH3)C(CH3)3、CH3CH(CH3)C(CH3)2CH2CH3、CH3C(CH3)2CH2CH(CH3)2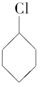 (一氯环己烷)$\stackrel{②}{→}$
(一氯环己烷)$\stackrel{②}{→}$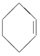 $→_{③}^{Br_{2}的CCl_{4}溶液}$B$\stackrel{④}{→}$
$→_{③}^{Br_{2}的CCl_{4}溶液}$B$\stackrel{④}{→}$