题目内容
19.33.5g Na2O2吸收CO2后,其质量增加到36.3g,则被吸收的CO2的质量是( )| A. | 4.4 g | B. | 2.2 g | C. | 5.5 g | D. | 8.2 g |
分析 发生反应:2Na2O2+2CO2=2Na2O3+O2,根据固体质量差量法计算参加反应二氧化碳的质量.
解答 解:设被吸收的CO2的质量是m,则:
2Na2O2+2CO2=2Na2O3+O2 固体质量增重△m
88 88-32=56
m 36.3g-33.5g=2.8g
所以m=$\frac{2.8g×88}{56}$=4.4g
故选:A.
点评 本题考查化学方程式计算,难度不大,注意根据质量守恒规律理解质量差量法.

练习册系列答案
相关题目
9.在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
| A. | 2H2(g)+O2(g)═2H2O(g)△H1 2H2(g)+O2(g)═2H2O(l)△H2 | |
| B. | S(s)+O2(g)═SO2(g)△H1 S(g)+O2(g)═SO2(g)△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1 C(s)+O2(g)═CO2(g)△H2 | |
| D. | H2(g)+Cl2(g)═2HCl(g)△H1 $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H2 |

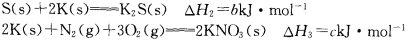
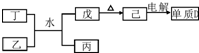
 ,
,