题目内容
已知硫化氢气体可与溴水反应生成硫,下图是用来制取硫化氢并比较硫元素、溴元素非金属性强弱的实验装置。 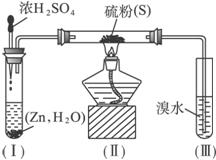
(1)将下列操作步骤补充完整:
①_____________________________________________________;
②用大火加热使硫沸腾与H2化合;
③_____________________________________________________;
④停止加热并做善后处理。
(2)装置(Ⅰ)中制氢气不直接用稀硫酸与锌反应,而将浓H2SO4滴入水中,其优点是
________________________________________________。
(3)装置(Ⅲ)中发生的现象是____________________________________,由此得出的结论是________________________,反应的离子方程式为____________________________。
(1)①检查装置气密性,挤压胶头滴管使H2SO4滴入试管,并检验H2的纯度
③待装置(Ⅲ)中的溴水褪色,并产生浑浊时撤去导管
(2)利用浓H2SO4溶于水时放出的热,加速H2的生成
(3)溴水褪色,产生淡黄色浑浊 溴的非金属性比硫强 Br2+H2S====S↓+2H++2Br-

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目