题目内容
按要求回答下列问题
(1)近年来,湖南省围绕“资源节约型和环境友好型”这一主题,积极谋求社会的和谐发展.请你根据这一主题和题意,用下列选项的字母代号进行填空.
A.二氧化硫 B.二氧化碳C.开发新能源D.沉淀法
a.造成温室效应和全球气候变暖的主要物质是 ;
b.以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的主要物质是 ;
c.水体污染加剧了水资源的短缺.处理含有Hg2+等重金属离子的废水常用的一种方法是 ;
d.石油是一种重要能源,人类正面临着石油短缺的难题.请说出解决能源短缺问题的一种方法 .
(2)现有三组混和物:①汽油和水;②碘和四氯化碳;③硫酸钡和稀硫酸.分离以上各混和物的正确方法依次是: 、 、 .
(3)相同质量的NH3和H2S两种气体,它们所含的分子数目之比为 ,所含的氢原子质量之比为 ;欲配制1000mL 1.0mol/L 的稀硫酸溶液,需要质量分数为98%,密度为1.84g/cm3的浓硫酸 mL.
(1)近年来,湖南省围绕“资源节约型和环境友好型”这一主题,积极谋求社会的和谐发展.请你根据这一主题和题意,用下列选项的字母代号进行填空.
A.二氧化硫 B.二氧化碳C.开发新能源D.沉淀法
a.造成温室效应和全球气候变暖的主要物质是
b.以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的主要物质是
c.水体污染加剧了水资源的短缺.处理含有Hg2+等重金属离子的废水常用的一种方法是
d.石油是一种重要能源,人类正面临着石油短缺的难题.请说出解决能源短缺问题的一种方法
(2)现有三组混和物:①汽油和水;②碘和四氯化碳;③硫酸钡和稀硫酸.分离以上各混和物的正确方法依次是:
(3)相同质量的NH3和H2S两种气体,它们所含的分子数目之比为
考点:常见的生活环境的污染及治理,物质的量的相关计算,物质的分离、提纯的基本方法选择与应用
专题:
分析:(1)a、二氧化碳的大量排放会导致全球气候变暖,引起温室效应;
b、煤中含有硫元素,煤燃烧会产生大量的二氧化硫;
c、处理含有Hg2+等重金属离子的废水常用沉淀法;
d、解决能源问题有两条出路:一是要把现有的能源利用好,提高利用率;二是要积极开发新能源,寻找替代能源,特别是提高太阳能的利用率,开发新能源核能;
(2)①汽油和水互不相溶;
②碘和四氯化碳混溶,但沸点不同;
③硫酸钡不溶于稀硫酸;
(3)根据n=
计算NH3和H2S气体的物质的量之比,同温同压下,气体体积之比等于其物质的量之比,结合每个分子含有原子数目之比计算氢原子的个数比;
根据c=
计算浓硫酸物质的量浓度,再根据稀释定律计算需要浓硫酸的体积;
b、煤中含有硫元素,煤燃烧会产生大量的二氧化硫;
c、处理含有Hg2+等重金属离子的废水常用沉淀法;
d、解决能源问题有两条出路:一是要把现有的能源利用好,提高利用率;二是要积极开发新能源,寻找替代能源,特别是提高太阳能的利用率,开发新能源核能;
(2)①汽油和水互不相溶;
②碘和四氯化碳混溶,但沸点不同;
③硫酸钡不溶于稀硫酸;
(3)根据n=
| m |
| M |
根据c=
| 1000ρω |
| M |
解答:
解:(1)a、二氧化碳的大量排放会导致全球气候变暖,引起温室效应,故答案为:B;
b、煤中含有硫元素,煤燃烧会产生大量的二氧化硫,二氧化硫是形成这类酸雨的主要物质,故答案为:A;
c、处理含有Hg2+等重金属离子的废水常用沉淀法,如加入硫化钠等,故选:D;
d、解决能源短缺问题可以开发新能源,寻找替代能源,故选:C;
(2)①汽油和水互不相溶,混合分层,利用分液分离;
②碘和四氯化碳混溶,但沸点不同,则利用蒸馏分离;
③硫酸钡不溶于稀硫酸,则利用过滤分离,
故答案为:分液;蒸馏;过滤;
(3)根据n=
可知,同质量的NH3和H2S气体的物质的量之比为34g/mol:17g/mol=2:1,同温同压下,分子数目之比等于其物质的量之比,故二者分子数目之比为2:1,含有氢原子的个数之比为2×3:1×2=3:1,
质量分数为98%、密度为1.84g/cm3的浓硫酸的物质的量浓度为
mol/L=18.4mol/L,配制1000mL 1.0mol/L的稀硫酸需要浓硫酸体积为
=54.3mL,
故答案为:2:1;3:1;54.3
b、煤中含有硫元素,煤燃烧会产生大量的二氧化硫,二氧化硫是形成这类酸雨的主要物质,故答案为:A;
c、处理含有Hg2+等重金属离子的废水常用沉淀法,如加入硫化钠等,故选:D;
d、解决能源短缺问题可以开发新能源,寻找替代能源,故选:C;
(2)①汽油和水互不相溶,混合分层,利用分液分离;
②碘和四氯化碳混溶,但沸点不同,则利用蒸馏分离;
③硫酸钡不溶于稀硫酸,则利用过滤分离,
故答案为:分液;蒸馏;过滤;
(3)根据n=
| m |
| M |
质量分数为98%、密度为1.84g/cm3的浓硫酸的物质的量浓度为
| 1000×1.84×98% |
| 98 |
| 1000mL×1mol/L |
| 18.4mol/L |
故答案为:2:1;3:1;54.3
点评:本题考查物质的分离、提纯以及溶液浓度有关计算,为高频考点,注意把握相关物质的性质的异同,把握操作方法和注意事项以及理解掌握物质的量浓度与质量分数之间的关系,学习中注意相关基础知识的积累,题目难度不大.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
钢铁在潮湿的空气中会被腐蚀,会发生的原电池反应.以下说法正确的是( )
| A、负极发生的反应为:Fe-3e-=Fe3+ |
| B、正极发生的反应为:2H2O+O2+4e-=4OH? |
| C、原电池是将电能转变为化学能的装置 |
| D、钢铁在水下部分比在空气与水交界处更容易腐蚀 |
下列说法正确的是( )
| A、垃圾处理常用的方法是卫生填埋、堆肥和焚烧 |
| B、将垃圾分类并回收是处理的发展方向 |
| C、填埋垃圾不需要治理,只需深埋即可 |
| D、垃圾是污染物,不会产生二次污染 |
下列各分子中所有原子都满足最外层为8电子结构的是( )
| A、H2O |
| B、BF3 |
| C、CCl4 |
| D、C2H6 |
照反应Br+H2?HBr+H的能量变化示意图,下列叙述正确的是( )
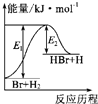

| A、该反应的△H=+(E1-E2)kJ?mol-1 |
| B、加入催化剂,该化学反应的反应热变大 |
| C、反应物的总能量高于生成物的总能量 |
| D、该反应为放热反应 |
设阿伏加德罗常数为NA,则下列说法正确的是( )
| A、15g甲基(-CH3)所含有的电子数是10NA | ||
| B、0.5mol 1,3一丁二烯分子中含有的碳碳双键数为NA | ||
C、标准状况下,1 L戊烷充分燃烧后生成的气态产物的分子数为
| ||
| D、60gSiO2晶体中,含有NA个Si-O键 |
