题目内容
下列溶液中有关物质的量浓度关系正确的是( )
| A、25℃时pH=12的NaOH溶液与pH=12的氨水中:c(Na+)>c(NH4+) |
| B、Na2CO3和NaHCO3混合溶液中一定有:2c(CO32-)+c(OH-)+c(HCO3-)=c(H+)+c(Na+) |
| C、pH=4的0.1mol?L-1的NaHA溶液中:c(HA-)>c(H+)>c(H2A)>c(A2-) |
| D、将①pH=2的CH3COOH溶液、②pH=2的盐酸、③0.01mol/L的氨水、④0.01mol/L的NaOH溶液,分别稀释100倍后溶液中的c(H+):②>①>④>③ |
考点:离子浓度大小的比较,盐类水解的应用,酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:A.溶液中存在电荷守恒,根据电荷守恒判断;
B.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
C.pH=4的0.1mol?L-1的NaHA溶液中,HA-的电离程度大于水解程度;
D.溶液稀释促进弱电解质电离,酸中氢离子浓度大于碱.
B.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
C.pH=4的0.1mol?L-1的NaHA溶液中,HA-的电离程度大于水解程度;
D.溶液稀释促进弱电解质电离,酸中氢离子浓度大于碱.
解答:
解:A.溶液中存在电荷守恒,根据电荷守恒得c(H+)+c(Na+)=c(H+)+c(NH4+)=c(OH-),溶液中c(H+)相等,则c(Na+)=c(NH4+),故A错误;
B.任何电解质溶液中都存在电荷守恒,根据电荷守恒得2c(CO32-)+c(OH-)+c(HCO3-)=c(H+)+c(Na+),故B正确;
C.pH=4的0.1mol?L-1的NaHA溶液中,HA-的电离程度大于水解程度,则c(H2A)<c(A2-),故C错误;
D.溶液稀释促进弱电解质电离,酸中氢离子浓度大于碱,①pH=2的CH3COOH溶液、②pH=2的盐酸稀释100倍后促进醋酸电离,导致醋酸中氢离子浓度大于盐酸,则醋酸中氢离子浓度大于盐酸;③0.01mol/L的氨水、④0.01mol/L的NaOH溶液,分别稀释100倍后,促进一水合氨电离,氨水溶液中氢氧根离子浓度大于NaOH,氢氧根离子浓度越大氢离子浓度越小,所以这几种溶液中氢离子浓度大小顺序是:①>②>④>③,故D错误;
故选B.
B.任何电解质溶液中都存在电荷守恒,根据电荷守恒得2c(CO32-)+c(OH-)+c(HCO3-)=c(H+)+c(Na+),故B正确;
C.pH=4的0.1mol?L-1的NaHA溶液中,HA-的电离程度大于水解程度,则c(H2A)<c(A2-),故C错误;
D.溶液稀释促进弱电解质电离,酸中氢离子浓度大于碱,①pH=2的CH3COOH溶液、②pH=2的盐酸稀释100倍后促进醋酸电离,导致醋酸中氢离子浓度大于盐酸,则醋酸中氢离子浓度大于盐酸;③0.01mol/L的氨水、④0.01mol/L的NaOH溶液,分别稀释100倍后,促进一水合氨电离,氨水溶液中氢氧根离子浓度大于NaOH,氢氧根离子浓度越大氢离子浓度越小,所以这几种溶液中氢离子浓度大小顺序是:①>②>④>③,故D错误;
故选B.
点评:本题考查了离子浓度大小比较,明确溶液中的溶质及其性质是解本题关键,再结合电荷守恒来分析解答,题目难度中等.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
下列各组物质的性质变化正确的是( )
| A、酸性HClO4>H3PO4>HNO3>H2SiO4 |
| B、稳定性H2S>HCl>HBr>HI |
| C、还原性Rb>K>Na>Li |
| D、碱性Al(OH)3>Mg(OH)2>NaOH |
下列各溶液中能大量共存的离子组是( )
| A、碳酸氢钠溶液中:K+、SO42-、Cl-、H+ |
| B、使pH试纸呈红色的溶液中:Fe2+、I-、NO3-、Cl- |
| C、使酚酞试液呈红色的溶液中:Mg2+、Cu2+、SO42-、K+ |
| D、c(H+)=10-14mol/L的溶液中:Na+、AlO2-、S2-、SO32- |
 硼化钒-空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时的反应为:4VB2+11O2═4B2O3+2V2O5,下列说法正确的是( )
硼化钒-空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时的反应为:4VB2+11O2═4B2O3+2V2O5,下列说法正确的是( )| A、电极a是电源负极 |
| B、溶液中的OH向a极移动 |
| C、电子由VB2极经KOH溶液流向电极a |
| D、VB2极发生的电极反应为:2VB2+22OH-═V2O5+2B2O3+11H2O+22e- |
一定温度下,某容积固定的密闭容器中发生反应:N2(g)+3H2(g)?2NH3(g)下列叙述中说明该反应达到化学平衡状态的是( )
| A、v(N2):v(H2):v(NH3)=1:3:2 |
| B、c(N2):c(H2):c(NH3)=1:3:2 |
| C、容器内混合气体的平均相对分子质量不变 |
| D、单位时间里每增加1molN2,同时增加3molH2 |
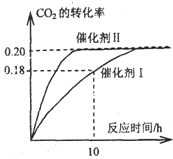 I.已知CO2可以生产绿色燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H=-87.4kJ?mol-1.300℃时,在一定容积的密闭容器中,当c(CO2)=1.00kJ?mol-1、c(H2)=1.60kJ?mol-1开始反应,结果如图所示,回答下列问题:
I.已知CO2可以生产绿色燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H=-87.4kJ?mol-1.300℃时,在一定容积的密闭容器中,当c(CO2)=1.00kJ?mol-1、c(H2)=1.60kJ?mol-1开始反应,结果如图所示,回答下列问题:
