题目内容
已知M是一种金属单质,F为红棕色固体,试根据下列框图中的关系回答有关问题:
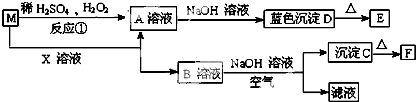
(1)出反应①的化学方程式
(2)“绿色化学”角度考虑,由M转化到A溶液的方法还有
(3)检验X溶液中主要阳离子的实验方法是
(4)出由B溶液到沉淀C的总离子方程式
(5)写出E、F的用途各一种:E 、F .

(1)出反应①的化学方程式
(2)“绿色化学”角度考虑,由M转化到A溶液的方法还有
(3)检验X溶液中主要阳离子的实验方法是
(4)出由B溶液到沉淀C的总离子方程式
(5)写出E、F的用途各一种:E
考点:无机物的推断
专题:推断题
分析:F为红棕色固体,则F为Fe2O3,沉淀C加热得到F,故C为Fe(OH)3,B与氢氧化钠溶液、氧气反应得到C,则B含有亚铁离子,M是一种金属单质,与稀硫酸、过氧化氢反应得到A,A与氢氧化钠溶液得到D为蓝色沉淀,D为Cu(OH)2,则M为Cu、A为CuSO4,D加热得到E,故E为CuO,M与X反应得到A与B,则B为FeSO4,X为Fe2(SO4)3,据此解答.
解答:
解:F为红棕色固体,则F为Fe2O3,沉淀C加热得到F,故C为Fe(OH)3,B与氢氧化钠溶液、氧气反应得到C,则B含有亚铁离子,M是一种金属单质,与稀硫酸、过氧化氢反应得到A,A与氢氧化钠溶液得到D为蓝色沉淀,D为Cu(OH)2,则M为Cu、A为CuSO4,D加热得到E,故E为CuO,M与X反应得到A与B,则B为FeSO4,X为Fe2(SO4)3,
(1)反应①的化学方程式为:Cu+H2SO4+H2O=CuSO4+2H2O,故答案为:Cu+H2SO4+H2O=CuSO4+2H2O;
(2)“绿色化学”角度考虑,由Cu转化到硫酸铜溶液的方法还有:将Cu粉加入稀硫酸中,边加热边通入空气(或将Cu在空气中加热完全转化为CuO,再加稀硫酸溶解),
故答案为:将Cu粉加入稀硫酸中,边加热边通入空气(或将Cu在空气中加热完全转化为CuO,再加稀硫酸溶解);
(3)X为Fe2(SO4)3,检验其溶液中主要阳离子的实验方法是:取少量X溶液于试管中,滴加几滴KSCN溶液,溶液变为红色,说明含有Fe3+,
故答案为:取少量X溶液于试管中,滴加几滴KSCN溶液,溶液变为红色,说明含有Fe3+;
(4)由B溶液到沉淀C的总离子方程式为:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓,故答案为:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓;
(5)E为CuO,可以制备铜盐,F为Fe2O3,可以用作红色涂料,故答案为:制备铜盐;红色涂料.
(1)反应①的化学方程式为:Cu+H2SO4+H2O=CuSO4+2H2O,故答案为:Cu+H2SO4+H2O=CuSO4+2H2O;
(2)“绿色化学”角度考虑,由Cu转化到硫酸铜溶液的方法还有:将Cu粉加入稀硫酸中,边加热边通入空气(或将Cu在空气中加热完全转化为CuO,再加稀硫酸溶解),
故答案为:将Cu粉加入稀硫酸中,边加热边通入空气(或将Cu在空气中加热完全转化为CuO,再加稀硫酸溶解);
(3)X为Fe2(SO4)3,检验其溶液中主要阳离子的实验方法是:取少量X溶液于试管中,滴加几滴KSCN溶液,溶液变为红色,说明含有Fe3+,
故答案为:取少量X溶液于试管中,滴加几滴KSCN溶液,溶液变为红色,说明含有Fe3+;
(4)由B溶液到沉淀C的总离子方程式为:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓,故答案为:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓;
(5)E为CuO,可以制备铜盐,F为Fe2O3,可以用作红色涂料,故答案为:制备铜盐;红色涂料.
点评:本题考查无机物推断,物质的颜色是推断突破口,再结合转化关系推断,需要学生熟练掌握元素化合物知识,难度中等.

练习册系列答案
相关题目
对于常温下pH为1的硝酸溶液,下列叙述正确的是( )
| A、硝酸为弱电解质 |
| B、该溶液1 mL稀释至100 mL后,pH小于3 |
| C、向该溶液中加入等体积、等浓度的氢氧化钡溶液,混合后溶液pH=7 |
| D、该溶液中水电离出的c(H+)=1×10-13 mol/L |
反应A(g)+3B(g)?2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是( )
| A、v (C)=30 mol/(L?min) |
| B、v (D)=0.4 mol/(L?s) |
| C、v (B)=0.6 mol/(L?s) |
| D、v (A)=12 mol/(L?min) |
下列说法正确的是( )
| A、光导纤维的主要成分是硅,可广泛用于通信和医疗领域 |
| B、水晶和金刚石都是由碳元素组成的宝石 |
| C、氮化硅、光导纤维等属于新型无机非金属材料 |
| D、合金的熔点一般比组成合金的各成分金属高 |
某酸性溶液中存在较多的Fe3+,则溶液中还可能大量存在的离子组是( )
| A、OH-、Cl-、Na+ |
| B、SO42-、Cl-、NH4+ |
| C、ClO-、HCO3-、K+ |
| D、I一、Fe2+、Ba2+ |
下列物质性质变化规律正确的是( )
| A、金属Na、Mg、Al的硬度依次降低 |
| B、HI、HBr、HCl、HF的稳定性依次减弱 |
| C、干冰、钠、冰的熔点依次降低 |
| D、O、F、H的原子半径依次减小 |