题目内容
黄铜矿(主要成分CuFeS2)是提取铜的主要原料
已知 CuFeS2+O2
Cu2S+SO2+FeO(炉渣)
已知产物Cu2S在1200℃高温下能继续反应:
Cu2S+O2→Cu2O+SO2 Cu2O+Cu2S→Cu+SO2
假定各步反应都完全,CuFeS2物质的量为2mol,O2的物质的量为a mol,请填写下列表格中(1)(2)(3)(4)空格内所表示的相关内容:
(1) (2) (3) (4) .
已知 CuFeS2+O2
| 800℃ |
已知产物Cu2S在1200℃高温下能继续反应:
Cu2S+O2→Cu2O+SO2 Cu2O+Cu2S→Cu+SO2
假定各步反应都完全,CuFeS2物质的量为2mol,O2的物质的量为a mol,请填写下列表格中(1)(2)(3)(4)空格内所表示的相关内容:
| 序号 | 1 | 2 | 3 | 4 | 5 | 6 |
| n(O2)的量 | a=4 | (3) | A≥5.5 | |||
| 残留固体 中含铜物质 | CuFeS2 Cu2S | (2) | Cu Cu2S | Cu | Cu Cu2O | |
| 物质的量 分别是多少 | (1) | (4) |
考点:有关混合物反应的计算,化学方程式的有关计算
专题:计算题
分析:根据化合价变化相等配平后的反应为:2CuFeS2+4O2
Cu2S+3SO2+2FeO(炉渣)、2Cu2S+3O2→2Cu2O+2SO2、2Cu2O+Cu2S→6Cu+SO2,
(1)根据反应2CuFeS2+4O2
Cu2S+3SO2+2FeO可知,当a<4mol时,氧气不足,则CuFeS2有剩余,残留固体中含铜物质为CuFeS2和Cu2S,根据反应计算出 其物质的量;
(2)当a=4mol时,CuFeS2和O2恰好反应:2CuFeS2+4O2
Cu2S+3SO2+2FeO,根据方程式判断残留固体中含铜物质;
(3)根据反应2CuFeS2+4O2
Cu2S+3SO2+2FeO(炉渣)、2Cu2S+3O2→2Cu2O+2SO2、2Cu2O+Cu2S→6Cu+SO2可得总反应:6CuFeS2+15O2=6Cu+12SO2+6FeO,当a=2mol×
=5mol,残留固体中含铜物质只有Cu,据此判断残留固体中含铜物质为Cu、Cu2S时a的范围;
(4)根据反应2CuFeS2+4O2
Cu2S+3SO2+2FeO(炉渣)、2Cu2S+3O2→2Cu2O+2SO2可得4CuFeS2+11O2=2Cu2O+8SO2+4FeO,当a≥2mol×
=5.5mol时,CuFeS2和O2恰好反应生成Cu2O,根据反应方程式计算出n(Cu2O).
| 800℃ |
(1)根据反应2CuFeS2+4O2
| 800℃ |
(2)当a=4mol时,CuFeS2和O2恰好反应:2CuFeS2+4O2
| 800℃ |
(3)根据反应2CuFeS2+4O2
| 800℃ |
| 15 |
| 6 |
(4)根据反应2CuFeS2+4O2
| 800℃ |
| 11 |
| 4 |
解答:
解:根据化合价变化相等配平后的反应为:2CuFeS2+4O2
Cu2S+3SO2+2FeO(炉渣)、2Cu2S+3O2→2Cu2O+2SO2、2Cu2O+Cu2S→6Cu+SO2,
(1)根据反应2CuFeS2+4O2
Cu2S+3SO2+2FeO可知,当a<4mol时,氧气不足,则CuFeS2有剩余,反应生成的Cu2S为:amol×
=0.25a mol,根据铜原子守恒可得剩余的CuFeS2为:2mol-0.25a mol×2=(2-0.5a)mol,
故答案为:n(CuFeS2)=2-0.5a、n(Cu2S)=0.25a;
(2)当a=4mol时,CuFeS2和O2恰好反应:2CuFeS2+4O2
Cu2S+3SO2+2FeO,残留固体中含铜物质为Cu2S,故答案为:Cu2S;
(3)根据反应2CuFeS2+4O2
Cu2S+3SO2+2FeO(炉渣)、2Cu2S+3O2→2Cu2O+2SO2、2Cu2O+Cu2S→6Cu+SO2可得总反应:6CuFeS2+15O2=6Cu+12SO2+6FeO,当a=2mol×
=5mol,残留固体中含铜物质只有Cu,所以残留固体中含铜物质为Cu、Cu2S时,4<a<5,
故答案为:4<a<5;
(4)根据反应2CuFeS2+4O2
Cu2S+3SO2+2FeO(炉渣)、2Cu2S+3O2→2Cu2O+2SO2可得4CuFeS2+11O2=2Cu2O+8SO2+4FeO,当a≥2mol×
=5.5mol时,CuFeS2和O2恰好反应生成Cu2O,根据质量守恒可得n(Cu2O)=1mol,
故答案为:n(Cu2O)=1mol.
| 800℃ |
(1)根据反应2CuFeS2+4O2
| 800℃ |
| 1 |
| 4 |
故答案为:n(CuFeS2)=2-0.5a、n(Cu2S)=0.25a;
(2)当a=4mol时,CuFeS2和O2恰好反应:2CuFeS2+4O2
| 800℃ |
(3)根据反应2CuFeS2+4O2
| 800℃ |
| 15 |
| 6 |
故答案为:4<a<5;
(4)根据反应2CuFeS2+4O2
| 800℃ |
| 11 |
| 4 |
故答案为:n(Cu2O)=1mol.
点评:本题考查了反应物过量的计算,题目难度较大,解答关键是根据分步反应正确书写总反应、然后根据反应物的量判断产物组成,试题培养了学生的分析、理解能力.

练习册系列答案
相关题目
导致下列现象主要与SO2的排放有关的是( )
| A、酸雨 | B、臭氧空洞 |
| C、温室效应 | D、白色污染 |
用Pt做电极,电解含C(Cu2+):C(Na+):C(Cl-)=1:2:4的混合溶液,在任何情况下,阴、阳两极下不可能同时发生的反应是( )
| A、阴极:2H++2e-=H2↑ 阳极:4OH--4e-=2H2O+O2↑ |
| B、阴极:2H++2e-=H2↑ 阳极:2Cl--2e-=Cl2↑ |
| C、阴极:Cu2++2e-=Cu 阳极:4OH--4e-=2H2O+O2↑ |
| D、阴极:Cu2++2e-=Cu 阳极:2Cl--2e-=Cl2↑ |
随着人们生活水平的不断提高,环保意识的增强,下列做法不科学的是( )
| A、购物时自带环保购物袋或竹篮 |
| B、大力发展清洁能源,如太阳能、氢能、风能等等 |
| C、出门尽量步行或者乘坐公交车,少开私家车 |
| D、随意丢弃废旧电池 |
能正确表示下列反应的离子反应方程式为( )
| A、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O |
| B、向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
| C、大理石溶于醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O |
| D、向明矾(KAl(SO4)2?12H2O)溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
0.1moL的某羧酸完全燃烧时,产生二氧化碳和水共3.4mol,该羧酸是( )
| A、C15H27COOH |
| B、C15H31COOH |
| C、C17H31COOH |
| D、C17H33COOH |
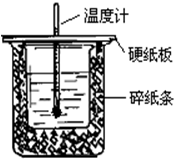 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: