题目内容
下列离子方程式书写正确的是( )
| A、.将少量金属钠放入冷水中:Na+2H2O=Na++2OH-+H2↑ | ||||
| B、向氯化铁溶液中加入铜:2Fe3++3Cu=2Fe+3Cu2+ | ||||
| C、向氯化铝溶液中加入过量氨水:Al3++4NH3?H2O=[Al(OH)4]--+4NH4+ | ||||
D、向二氧化锰中滴加浓盐酸并加热:MnO2+4H++2Cl-
|
考点:离子方程式的书写
专题:离子反应专题
分析:A、选项中电荷不守恒;
B、铜和氯化铁溶液反应生成氯化亚铁和氯化铜;
C、氢氧化铝不溶于过量氨水中;
D、二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水,二氧化锰是氧化物.
B、铜和氯化铁溶液反应生成氯化亚铁和氯化铜;
C、氢氧化铝不溶于过量氨水中;
D、二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水,二氧化锰是氧化物.
解答:
解:A、选项中电荷不守恒,将少量金属钠放入冷水中反应的离子方程式:2Na+2H2O=2Na++2OH-+H2↑,故A错误;
B、铜和氯化铁溶液反应生成氯化亚铁和氯化铜,反应的离子方程式2Fe3++Cu=2Fe2++Cu2+,故B错误;
C、氢氧化铝不溶于过量氨水中,向氯化铝溶液中加入过量氨水反应的离子方程式:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故C错误;
D、二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水,二氧化锰是氧化物,反应的离子方程式为MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故D正确;
故选D.
B、铜和氯化铁溶液反应生成氯化亚铁和氯化铜,反应的离子方程式2Fe3++Cu=2Fe2++Cu2+,故B错误;
C、氢氧化铝不溶于过量氨水中,向氯化铝溶液中加入过量氨水反应的离子方程式:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故C错误;
D、二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水,二氧化锰是氧化物,反应的离子方程式为MnO2+4H++2Cl-
| ||
故选D.
点评:本题考查了离子方程式书写方法和注意问题,主要是电荷守恒分析,注意氢氧化铝不溶于弱酸,弱碱,题目较简单.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
下列离子在溶液中能大量共存的是( )
| A、CO32-、Na+、SO42-、H+ |
| B、Cu2+、SO42-、H+、Cl- |
| C、K+、OH-、NO3-、HCO3- |
| D、Al3+、NO3-、SO42-、OH- |
请用下列装置进行下列实验,可以达到实验目的是( )
A、 定量测定化学反应速率 |
B、 验证钠与水反映的热效应 |
C、 加热d即可进行乙醇的催化氧化实验 |
D、 比较Fe3+和Cu2+对H2O2分解的催化效果 |
已知NH4++AlO2-+2H2O=Al(OH)3↓+NH3?H2O.向含有等物质的量的NH4Cl、AlCl3和HCl混合溶液中慢慢滴加NaOH溶液至过量,并不断搅拌,可能发生以下离子反应:①H++OH-=H2O;②Al(OH)3+OH-=AlO2-+2H2O;③Al3++3OH-=Al(OH)3↓;④NH4++OH-=NH3?H2O;⑤NH4++AlO2-+2H2O=Al(OH)3↓+NH3?H2O.其正确的离子反应顺序是( )
| A、①③②④ | B、①③④② |
| C、①③②⑤ | D、①④③② |
下列说法中正确的是( )
| A、500mL 1mol?L-1 MgCl2溶液中含有Cl-数目为0.5NA |
| B、标准状况下,1mol H2O与1mol O2所占的体积相等 |
| C、1mol S与足量Cu反应生成Cu2S,转移的电子数为NA |
| D、常温常压下,1mol氦气所含的原子数为NA |
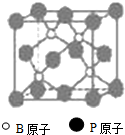 (物质结构与性质)磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,右下图为磷化硼晶体结构中最小的重复结构单元.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成:BBr3+PBr3+3H2=BP+6HBr.
(物质结构与性质)磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,右下图为磷化硼晶体结构中最小的重复结构单元.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成:BBr3+PBr3+3H2=BP+6HBr. (1)北京奥运会的“祥云”火炬所用燃料主要是丙烷,若以硫酸溶液为电解质溶液,两极分别通入丙烷和空气,形成燃料电池,则反应总方程式为
(1)北京奥运会的“祥云”火炬所用燃料主要是丙烷,若以硫酸溶液为电解质溶液,两极分别通入丙烷和空气,形成燃料电池,则反应总方程式为