题目内容
18.固体硝酸盐加热易分解且产物较复杂.某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想:甲:Mg(NO2)2、NO2、O2乙:MgO、NO2、O2 丙:Mg3N2、O2丁:MgO、NO2、N2
(1)实验前,小组成员经讨论认定猜想丁不成立,理由是不符合氧化还原反应原理
查阅资料得知:2NO2+2NaOH═NaNO3+NaNO2+H2O
针对甲、乙、丙猜想,设计如图所示的实验装置(图中加热、夹持仪器等均省略):
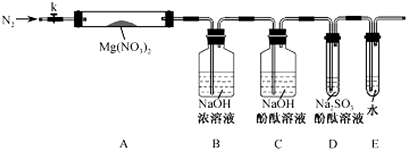
(2)实验过程
①取器连接后,放人固体试剂之前,关闭k,微热硬质玻璃管(A),观察到E 中有气泡连续放出,表明装置气密性良好
②称取Mg(NO3)2固体3.79g置于A中,加热前通人N2以驱尽装置内的空气,其目的是避免对产物O2检验产生干扰(或其它合理答案);关闭K,用酒精灯加热时,正确操作是先移动酒精灯预热硬质玻璃管然后固定在管中固体部位下加热.
③观察到A 中有红棕色气体出现,C、D 中未见明显变化.
④待样品完全分解,A 装置冷却至室温、称量,测得剩余固体的质量为1.0g
⑤取少量剩余固体于试管中,加人适量水,未见明显现象.
(3)实验结果分析讨论
①根据实验现象和剩余固体的质量经分析可初步确认猜想乙是正确的.
②根据D 中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中将发生氧化还原反应:2Na2SO3+O2=2Na2SO4(填写化学方程式),溶液颜色会退去;小组讨论认定分解产物中有O2存在,未检侧到的原因是O2在通过装置B时已参与反应(或其它合理答案)
③小组讨论后达成的共识是上述实验设计仍不完善,需改进装里进一步研究.
分析 (1)根据氧化还原反应化合价升降相等判断;
(2)①反应前检验装置的气密性;
②甲、乙、丙中都有氧气,避免空气中氧气干扰;根据加热试管的操作要求完成;
(3)①根据硝酸镁的反应现象进行判断;
②D中亚硫酸钠具有还原性,能够和氧气反应生成硫酸钠,溶液褪色;二氧化氮和氢氧化钠溶液反应生成一氧化氮,一氧化氮会消耗氧气.
解答 解:(1)由于产物中化合价只有降低情况,没有升高,不满足氧化还原反应的特征,
故答案为:不符合氧化还原反应原理(或其它合理答案);
(2)①实验前需要检验装置的气密性,方法是关闭k,微热硬质玻璃管(A),观察到E中有气泡连续放出,证明装置气密性良好,
故答案为:装置气密性良好;
②由于甲乙丙猜想中产物都有氧气,没有氮气,用氮气排出装置中空气避免对产物氧气检验的干扰,
集中加热前先预热硬质试管,然后固定在管中固体部位下加热,
故答案为:避免对产物O2检验产生干扰(或其它合理答案);移动酒精灯预热硬质玻璃管;
(3)①硝酸镁分解,红棕色气体是二氧化氮,镁元素不会还是硝酸镁形式,所以乙正确;
故答案为:乙;
②亚硫酸钠和氧气的反应,反应方程式是:2Na2SO3+O2=2Na2SO4,
在B装置中,二氧化氮和氢氧化钠溶液反应生成一氧化氮,生成的一氧化氮消耗了氧气,
故答案为:2Na2SO3+O2=2Na2SO4;O2在通过装置B时已参与反应(或其它合理答案).
点评 本题探究硝酸镁分解产物,提出假想,通过实验验证,涉及了化学方程式的书写、加热操作的考查,本题难度中等.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
9.下列说法中一定正确的是( )
| A. | pH=7的溶液呈中性 | |
| B. | pH值为0的溶液中c(H+)=0 mol/L | |
| C. | pH=5的溶液中[H+]=1.0×10-5 mol•L-1 | |
| D. | pH=5的溶液中[OH-]=1.0×10-9 mol•L-1 |
13.下列有关离子方程式的书写正确的是( )
| A. | NaHCO3溶液和盐酸;CO32-+2H+═H2O+CO2↑ | |
| B. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ | |
| C. | 向硫化钠溶液中滴入氯化铝溶液:2Al3++3S2-═Al2S3↓ | |
| D. |  溶液通入少量CO2: 溶液通入少量CO2: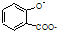 +CO2+H2O→ +CO2+H2O→ +HCO3- +HCO3- |
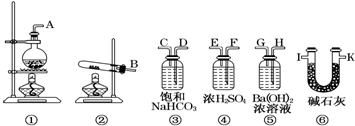
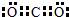 ,Z3+的原子结构示意图为
,Z3+的原子结构示意图为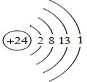
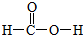 ,m g该物质完全燃烧后通过足量Na2O2固体吸收,Na2O2固体增重的质量为$\frac{15m}{23}$g.
,m g该物质完全燃烧后通过足量Na2O2固体吸收,Na2O2固体增重的质量为$\frac{15m}{23}$g. 某研究小组为探究SO2和Fe(NO3)3溶液的反应的实质.设计了如图所示装置进行实验.已知:1.0mol/L的Fe(NO3)3溶液的pH=1.
某研究小组为探究SO2和Fe(NO3)3溶液的反应的实质.设计了如图所示装置进行实验.已知:1.0mol/L的Fe(NO3)3溶液的pH=1.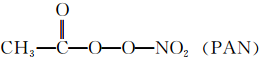 等二次污染物.
等二次污染物.