题目内容
5.下列说法正确的是( )| A. | AlCl3溶液和Al2(SO4)3溶液加热、蒸发、浓缩、结晶、灼烧,所得固体成分相同 | |
| B. | 1L 1mol/L的Na2S溶液中Na与S2-数目总和小于3NA(NA表示阿伏加德罗常数) | |
| C. | NH4Cl溶液加水稀释后,恢复至原温度,pH和Kw均增大 | |
| D. | 常温下,向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗衣净的沉淀中加稀盐酸,有气泡产生,因此Ksp(BaSO4)>Ksp(BaCO3) |
分析 A、氯化铝水解生成氢氧化铝和氯化氢,加热促进氯化氢挥发,从而促进氯化铝水解,硫酸铝水解生成氢氧化铝和硫酸;
B、Na2S溶液中硫离子会发生水解反应;
C、pH和Kw均只受温度的影响;
D、从难溶电解质的溶解平衡的角度分析.
解答 解:A、氯化铝水解生成氢氧化铝和氯化氢,加热促进氯化氢挥发,从而促进氯化铝水解,将溶液蒸干得到氢氧化铝固体,灼烧时氢氧化铝分解生成氧化铝和水蒸气,硫酸铝水解生成氢氧化铝和硫酸,加热促进硫酸铝水解,因为硫酸没有挥发性,所以得到的固体仍然是Al2(SO4)3,所得固体成分不相同,故A错误;
B、Na2S溶液中硫离子会发生水解反应,所以溶液中Na与S2-数目总和小于3NA,故B正确;
C、NH4Cl溶液加水稀释后,恢复至原温度,pH和Kw均不变,故C错误;
D、当c(Ba2+)•c(CO32-)>Ksp(BaCO3)时,可将BaSO4转化为BaCO3,但Ksp(BaCO3)>Ksp(BaSO4),故D错误.
故选B.
点评 本题综合考查盐的水解原理和应用、化学平衡常数、沉淀溶解平衡等知识,注意知识的迁移应用是关键,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列不属于配合物的是( )
| A. | [Cu(NH3)4]SO4•H2O | B. | [Ag(NH3)2]OH | C. | NH4NO3 | D. | Na[Al(OH)4] |
16.已知同一碳原子连有两个羟基不稳定: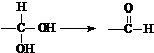
有机物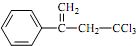 是选择性内吸传导性除草剂,俗称稗草烯,主要用于水稻田防除稗草,温度和湿度对药效影响大,温度高、湿度大药效发挥快.下列有关该有机物的说法正确的是( )
是选择性内吸传导性除草剂,俗称稗草烯,主要用于水稻田防除稗草,温度和湿度对药效影响大,温度高、湿度大药效发挥快.下列有关该有机物的说法正确的是( )
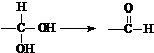
有机物
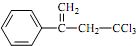 是选择性内吸传导性除草剂,俗称稗草烯,主要用于水稻田防除稗草,温度和湿度对药效影响大,温度高、湿度大药效发挥快.下列有关该有机物的说法正确的是( )
是选择性内吸传导性除草剂,俗称稗草烯,主要用于水稻田防除稗草,温度和湿度对药效影响大,温度高、湿度大药效发挥快.下列有关该有机物的说法正确的是( )| A. | 属于卤代烃,不能使酸性高锰酸钾溶液和溴水褪色 | |
| B. | 该物质存在顺反异构 | |
| C. | 在碱性条件下充分水解,可生成羧酸盐 | |
| D. | 1mol 该物质在一定条件下可与 3molH2发生加成反应 |
13.某有机物 X 的结构简式如图所示,则下列有关说法中正确的是( )


| A. | X的分子式为 C12H16O3 | |
| B. | X在核磁共振氢谱图中共出现8组峰 | |
| C. | X在一定条件下能发生加成、加聚、取代、氧化等反应 | |
| D. | 在Ni作催化剂的条件下,1mol X 最多只能与5molH2加成 |
20.FeCl2是一种常用的还原剂,实验室可以用多种方法来制备无水FeCl2.
I.按如图1装置用H2还原无水FeCl2制取.
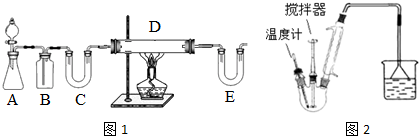
(1)装置C的作用是干燥氢气;E中盛放的试剂是碱石灰;D中反应的化学方程式为H2+2FeCl3$\frac{\underline{\;加热\;}}{\;}$2FeCl2+2HCl.
(2)若温度控制不当,产品中会含单质铁.检验产品中是否含铁的方案是取样,加入盐酸中,观察是否有气泡产生.
Ⅱ.按图2装置,在三颈烧瓶中放入162.5g无水氯化铁和225g氯苯,控制反应温度在128~139℃加热3h,反应接近100%.冷却,分离提纯得到粗产品.相关反应为2FeCl3+C6H5Cl→FeCl2+C6H4Cl2+HCl.有关数据如下:
(3)该制取反应中,作还原剂的是C6H5Cl.
(4)反应温度接近或超过C6H5Cl的沸点,但实验过程中C6H5Cl并不会大量损失.原因是实验使用了冷凝回流装置.
(5)冷却实验装置,将三颈瓶内物质经过过滤,洗涤沉淀并干燥后,得到粗产品.
①洗涤所用的试剂可以是苯;
②回收滤液中C6H5Cl的方案是蒸馏滤液,并收集132℃馏分.
(6)仅通过烧杯中的现象变化就可以监控氯化铁的转化率.若要监控氯化铁转化率已达到或超过90%,则烧杯中加入的试剂可以是滴有酚酞且含18gNaOH的溶液.
I.按如图1装置用H2还原无水FeCl2制取.

(1)装置C的作用是干燥氢气;E中盛放的试剂是碱石灰;D中反应的化学方程式为H2+2FeCl3$\frac{\underline{\;加热\;}}{\;}$2FeCl2+2HCl.
(2)若温度控制不当,产品中会含单质铁.检验产品中是否含铁的方案是取样,加入盐酸中,观察是否有气泡产生.
Ⅱ.按图2装置,在三颈烧瓶中放入162.5g无水氯化铁和225g氯苯,控制反应温度在128~139℃加热3h,反应接近100%.冷却,分离提纯得到粗产品.相关反应为2FeCl3+C6H5Cl→FeCl2+C6H4Cl2+HCl.有关数据如下:
| C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl、C6H4Cl2、苯,易吸水. | ||
| 熔点/℃ | -45 | 53 | -- | -- |
| 沸点/℃ | 132 | 173 | -- | -- |
(4)反应温度接近或超过C6H5Cl的沸点,但实验过程中C6H5Cl并不会大量损失.原因是实验使用了冷凝回流装置.
(5)冷却实验装置,将三颈瓶内物质经过过滤,洗涤沉淀并干燥后,得到粗产品.
①洗涤所用的试剂可以是苯;
②回收滤液中C6H5Cl的方案是蒸馏滤液,并收集132℃馏分.
(6)仅通过烧杯中的现象变化就可以监控氯化铁的转化率.若要监控氯化铁转化率已达到或超过90%,则烧杯中加入的试剂可以是滴有酚酞且含18gNaOH的溶液.
10.化学与生活密切相关.下列说法正确的是( )
| A. | 棉、蚕丝、合成纤维完全燃烧都只生成CO2和H2O | |
| B. | 牛奶、鸡蛋清均可用于重金属中毒解毒 | |
| C. | 白菜上洒少许福尔马林,既保鲜又消毒 | |
| D. | 氨水能导电,说明氨气是电解质 |
17.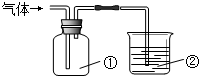 利用如图装置收集气体并验证其某些化学性质,正确的是( )
利用如图装置收集气体并验证其某些化学性质,正确的是( )
 利用如图装置收集气体并验证其某些化学性质,正确的是( )
利用如图装置收集气体并验证其某些化学性质,正确的是( )| 选项 | 气体 | 试剂② | 现象 | 结论 |
| A | NH3 | 酚酞试液 | 溶液变红色 | NH3的水溶液显碱性 |
| B | Cl2 | 紫色石蕊试液 | 溶液立即褪色 | Cl2有氧化性 |
| C | SO2 | 溴水 | 溶液褪色 | SO2有漂白性 |
| D | X(能形成酸雨) | KI淀粉溶液 | 溶液变蓝 | X是NO2 |
| A. | A | B. | B | C. | C | D. | D |
14.下列说法正确的是( )
| A. | 戊烷、戊醇、戊烯、乙酸乙酯中同分异构体数目最少的是戊烯 | |
| B. | 分子式为C4H9Cl的有机化合物有4种 | |
| C. | 丙烯与HCl在一定条件下的产物只有一种 | |
| D. | 用CH2(NH2)-COOH和CH3-CH(NH2)-COOH两种氨基酸脱水,最多可以生成3种2肽 |
15.已知X、Y、Z为第三周期元素,其原子的第一至第四电离能如表:
则X、Y、Z三种元素中原子半径最小的是Al(填元素符号),三种元素中有两种元素的最高价氧化物对应的水化物能相互反应,写出反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |