题目内容
己知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mo1-1,下列结论正确的是( )
| A、在密闭容器中加入1mol N2和3mol H2充分反应放热92.4kJ |
| B、N2(g)+3H2(g)?2NH3(l)△H=-QkJ?mo1-1,则Q>92.4 |
| C、增大压强,平衡向右移动,平衡常数增大 |
| D、若一定条件下反应达到平衡,N2的转化率为20%,则H2的转化率一定为60% |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A.该反应为可逆反应,反应物转化率不可能为100%,所以放出的热量小于92.4kJ;
B.气态氨气比液体氨含有的能量高,所以若生成液态氨气,则放出的热量大于92.4kJ;
C.温度不变,化学平衡常数不会变化;
D.氢气的转化率与初始加入的氢气的物质的量有关,根据氮气的转化率无法计算氢气的转化率.
B.气态氨气比液体氨含有的能量高,所以若生成液态氨气,则放出的热量大于92.4kJ;
C.温度不变,化学平衡常数不会变化;
D.氢气的转化率与初始加入的氢气的物质的量有关,根据氮气的转化率无法计算氢气的转化率.
解答:
解:A.该反应为可逆反应,在密闭容器中加入1mol N2和3mol H2充分反应后生成的氨气的物质的量小于2mol,放出的热量一定小于92.4kJ,故A错误;
B.N2(g)+3H2(g)?2NH3(l)△H=-QkJ?mo1-1,反应产物为液态,液态的氨气能量小于氨气能量,所以放出的热量大于92.4kJ,所以Q>92.4,故B正确;
C.增大压强,平衡向着正向移动,但是温度不变,该反应的平衡常数不变,故C错误;
D.氢气的初始量、反应消耗的氢气的物质的量不知,无法根据氮气的物质的量计算出氢气的转化率,若氮气和氢气的物质的量之比为1:3,则氮气的转化率与氢气的转化率相等,故D错误;
故选B.
B.N2(g)+3H2(g)?2NH3(l)△H=-QkJ?mo1-1,反应产物为液态,液态的氨气能量小于氨气能量,所以放出的热量大于92.4kJ,所以Q>92.4,故B正确;
C.增大压强,平衡向着正向移动,但是温度不变,该反应的平衡常数不变,故C错误;
D.氢气的初始量、反应消耗的氢气的物质的量不知,无法根据氮气的物质的量计算出氢气的转化率,若氮气和氢气的物质的量之比为1:3,则氮气的转化率与氢气的转化率相等,故D错误;
故选B.
点评:本题考查了反应热的计算、化学平衡的影响因素,题目难度中等,注意掌握化学平衡的影响因素及反应热的计算方法,明确可逆反应中反应物转化率不可能为100%.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
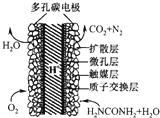 电化学化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于该电池描述正确的是( )
电化学化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于该电池描述正确的是( )| A、电池工作时H+移向负极 |
| B、该装置还可以将电能转化成为化学能 |
| C、电池的负极反应式为:CO(NH2)2+H2O-6e-=CO2+N2+6H+ |
| D、理论上电池工作时,每消耗67.2L O2时,可以净化2mol CO(NH2)2 |
下列各组离子在指定的溶液中可能大量共存的是( )
| A、使甲基橙变红色的溶液:K+、Al3+、MnO4-、C2O42- |
| B、加入铝产生氢气的溶液:H+、Mg2+、NO3-、SO42- |
| C、pH=12的溶液中:Na+、Ba2+、NO3-、Cl- |
| D、含Al2Fe(SO4)4的溶液:Na+、NH4+、S2O32-、ClO- |
十八大报告中提出“大力推进生态文明建设,提高生态文明水平,建设美丽中国”.化学已渗透到人类生活的各个方面.下列说法正确的是( )
| A、PM2.5是指大气中直径≤2.5微米的颗粒物,只要戴普通口罩就对人体健康无影响 |
| B、绚丽缤纷的烟花中可能添加了含钾、钠、钙、铜等某些金属元素的化合物 |
| C、乙醇、过氧化氢、次氯酸钠等消毒液均可以将病毒氧化而达到消毒的目的 |
| D、地沟油的主要成分是高级脂肪酸甘油酯,可用于制肥皂和加工食用油 |
以下反应最符合绿色化学,原子经济性要求的是( )
| A、乙烯聚合为聚乙烯高分子材料 |
| B、甲烷与氯气制备一氯甲烷 |
| C、以铜和浓硝酸为原料生产硝酸铜 |
| D、乙醇催化氧化制乙醛 |
下列离子方程式书写正确的是( )
| A、铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
| B、钠投入水中:Na+H2O═Na++2OH-+H2↑ |
| C、氯化铝溶液中加入过量氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
| D、氢氧化钡溶液滴入稀硫酸中:Ba2++OH-+H++SO42-═BaSO4↓+H2O |