题目内容
12.在化工生产常用的3种有机物①乙烯、②乙醇、③油脂中,可用于制取肥皂的是③(填序号,下同),可用来衡量一个国家石油化工发展水平的是①,可与水以任意比互溶的是②.分析 油脂在碱性条件下的水解反应称为皂化反应;乙烯是石油的综合利用过程中的重要产物,且是一种重要的基础化工原料;醇类能和水分子间形成氢键,据此分析.
解答 解:油脂在碱性条件下的水解能生成甘油和硬质酸钠,故油脂在碱性条件下的水解反应称为皂化反应,即油脂可以用于制造肥皂;乙烯是石油的综合利用过程中的重要产物,且是一种重要的基础化工原料,故可以用乙烯的产量来衡量一个国家的石油化工发展水平;醇类能和水分子间形成氢键,故乙醇能和水互溶,
故答案为:③;①;②.
点评 本题考查了化学中常见的有机物的用途以及在工业生产中的标志性作用,难度不大,应注意的是由于醇分子间、醇和水分子间存在氢键,故醇类的沸点较高,且能和水互溶.

练习册系列答案
相关题目
2.已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的原子序数依次增大.其中A、C原子的L层有2个未成对电子.D与E同主族,D的二价阳离子与C的阴离子具有相同的电子层结构.F3+离子M层3d轨道电子为半满状态.请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)写出F原子的外围电子排布式3d64s2.
(2)与A22-互为等电子体的单质是N2,A22-中成键原子的杂化类型是sp
(3)F和M(质子数为25)两元素的部分电离能数据列于右表:比较两元素的I2、I3可知,气态M2+再失去一个电子比气态F2+再失去一个电子难.对此,你的解释是:Mn2+的3d轨道电子排布为半满状态较稳定.
(4)H2S和C元素的氢化物(分子式为H2C2)的主要物理性质比较如下:
H2S和H2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因:H2O2分子间存在氢键,与水分子可形成氢键;
(5)如图a、b分别为M、F晶体的堆积模型,假设M的原子半径分别为Ranm,它的空间利用率:(不用化简)M$\frac{π}{3\sqrt{2}}$.
(1)写出F原子的外围电子排布式3d64s2.
| 元 素 | M | F | |
| 电离能 (kJ•mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(3)F和M(质子数为25)两元素的部分电离能数据列于右表:比较两元素的I2、I3可知,气态M2+再失去一个电子比气态F2+再失去一个电子难.对此,你的解释是:Mn2+的3d轨道电子排布为半满状态较稳定.
(4)H2S和C元素的氢化物(分子式为H2C2)的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 以任意比互溶 |
(5)如图a、b分别为M、F晶体的堆积模型,假设M的原子半径分别为Ranm,它的空间利用率:(不用化简)M$\frac{π}{3\sqrt{2}}$.

3.关于铜锌原电池(稀硫酸作电解质溶液)的叙述正确的是( )
| A. | 铜是负极,铜片上有气泡产生 | B. | 电流从锌片经导线流向铜片 | ||
| C. | H+在铜片表面被还原 | D. | 铜片质量逐渐减小 |
20.一定条件下能与CH4发生取代反应的是( )
| A. | Cl2 | B. | O2 | C. | 溴水 | D. | KMnO4酸性溶液 |
7.下列说法中,正确的是( )
| A. | 1 mol CO2的质量是44g | |
| B. | 17 g NH3的体积是22.4 L | |
| C. | 100 mL 1 mol/L NaOH溶液中含有1 mol OH- | |
| D. | 标准状况下,11.2 L O2中含有6.02×1023个氧分子 |
4.常温下,下列溶液的pH大于7的是( )
| A. | NH4Cl | B. | Al2(SO4)3 | C. | NaHCO3 | D. | Na2SO4 |
1.下列无色溶液中,能大量共存的一组是( )
| A. | Na+ Cu2+ Cl- SO42- | B. | Na+ Ca2+ CO32- NO3- | ||
| C. | Na+ H+ Cl- NO3- | D. | K+ H+ SO42- OH- |
2.如图为实验室中的蒸馏装置,下列有关说法正确的是( )
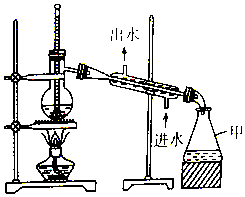

| A. | 仪器甲是锥形瓶,可直接用酒精灯加热 | |
| B. | 温度计水银球应该置于蒸馏烧瓶支管口处 | |
| C. | 直形冷凝管可用球形冷凝管代替 | |
| D. | 石油蒸馏时加沸石,制蒸馏水时不用加沸石 |
 ⑥
⑥