题目内容
某一固体物质可能由NaOH、AlCl3、MgCl2中的几种组成,取其一定量溶于水,有沉淀产生,在所得悬浊液中逐滴加入5mol/L的盐酸,下图表示盐酸加入量与沉淀量的变化关系,图中M点表示已加入的盐酸体积,则M点的体积是
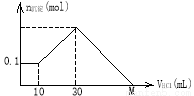
A.70mL B.100mL C.120mL D.130mL
D
【解析】
试题分析:向所得浊液中,逐滴加入5mol/L盐酸,由加入盐酸的体积和生成沉淀的质量关系图分析:
①0-10ml,随盐酸的体积增加,生成沉淀的质量不变,说明沉淀是Mg(OH)2,n=0.1mol,
由Na+离子和Cl-离子守恒得:n(NaOH)=n(NaCl)=n(Cl-)=2n(MgCl2)+3n(AlCl3)+n(HCl)=0.1mol×2+0.1mol×3+0.03L×5mol/L=0.65mol,M点溶液为MgCl2、AlCl3和NaCl混合液,M点所加盐酸相等于用于中和原混合物中的NaOH,此时所加盐酸物质的量:n(HCl)=n(NaOH)=0.65mol;M点所表示盐酸的体积为:V=0.65/5=0.13L=130ml。
考点:考查Mg(OH)2、Al(OH)3的性质。

(8分)某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5 mol·L-1盐酸、0.55 mol·L-1NaOH溶液,实验尚缺少的玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),其原因是 。
(3)他们记录的实验数据如下:
实验用品 | 溶液温度 | 中和热 | ||||
T1 | t2 | ΔH | ||||
① | 50 mL0.55 mol·L-1 NaOH溶液 | 50 mL0.5 mol·L-1 HCl溶液 | 20 ℃ | 23.3 ℃ |
| |
② | 50 mL0.55 mol·L-1 NaOH溶液 | 50 mL0.5 mol·L-1 HCl溶液 | 20 ℃ | 23.5 ℃ | ||
(已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18 kJ·℃-1·kg-1,各物质的密度均为1 g·cm-3。)
根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式: 。
(4)若用KOH代替NaOH,对测定结果 (填“有”或 “无”)影响;若用醋酸代替HCl做实验,对测定结果 (填“有”或“无”)影响。

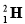 ②H2O、D2O ③
②H2O、D2O ③
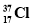 ④金刚石、石墨 ⑤O2、O3 ⑥H2、H+
④金刚石、石墨 ⑤O2、O3 ⑥H2、H+