题目内容
12.近年来我国汽车拥有量呈较快增长趋势,NOx是汽车尾气中的主要污染物之一(1)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
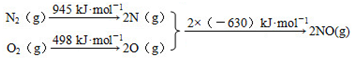
热化学方程式N2(g)+O2(g)=2NO(g)的△H=+183 kJ/mol,该反应的△S>0(填“>”、“<”或“=”);
(2)氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)═NaNO3(s)+ClNO(g) K1△H<0 (I)
2NO(g)+Cl2(g)═2ClNO(g) K2△H<0 (II)
①4NO2(g)+2NaCl(s)═2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=$\frac{{{K}_{1}}^{2}}{{K}_{2}}$(用K1、K2表示).
②为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(Ⅱ)达到平衡.测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则平衡后n(Cl2)=0.025mol,NO的转化率α1=75%.③其它条件保持不变,反应(II)在恒压条件下进行,平衡时NO的转化率α2>α1(填“>”“<”或“=”),平衡常数K2不变(填“增大”“减小”或“不变”,若要使K2减小,可采用的措施是升高温度.
(3)合成氨是人类科学技术上的一项重大突破,其反应原理为N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1.依据温度对合成氨反应的影响,在如图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图:

分析 (1)根据能量变化图计算反应热,反应热=反应物的键能和-生成物的键能和,标注物质聚集状态和对应反应焓变书写热化学方程式得到反应焓变,反应前后是气体体积不变的反应,反应自发进行的条件是△G=△H-T△S<0,非自发进行△G=△H-T△S>0,据此反应是非自发进行来判断熵变;
(2)①依据化学平衡常数概念,结合反应化学方程式书写反应的平衡常数,
2NO2(g)+NaCl(s)═NaNO3(s)+ClNO(g) K1△H<0 (I)
2NO(g)+Cl2(g)═2ClNO(g) K2△H<0 (II),
4NO2(g)+2NaCl(s)═2NaNO3(s)+2NO(g)+Cl2(g)结合平衡常数表达式计算得到平衡常数关系;
②依据平衡三段式列式计算,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(Ⅱ)达到平衡,测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,物质的量为7.5×10-3mol•L-1•min-1×10min×2L=0.15mol,
2NO(g)+Cl2(g)?2ClNO(g),
起始量(mol) 0.2 0.1 0
变化量(mol) 0.15 0.075 0.15
平衡量(mol) 0.05 0.025 0.15
依据反应速率概念、转化率概念的计算,计算V=$\frac{△c}{△t}$,转化率=$\frac{消耗量}{起始量}$×100%;
③反应(Ⅱ)在恒压条件下进行,随反应进行,气体体积减小,为保持恒压所以容器体积减小,压强比恒容容器大,平衡正向进行,平衡时NO的转化率α2 增大;平衡常数随温度变化,不随浓度、压强变化,若要使K2减小,平衡逆向进行,反应是放热反应,依据平衡移动原理应升高温度,平衡逆向进行,平衡常数随温度变化;
(3)合成氨的反应是放热反应,开始反应,氨气物质的量增大,达到平衡状态,继续升温,平衡逆向进行,氨气物质的量减小,据此画出变化图象;
解答 解:(1)该反应中的反应热=反应物的键能和-生成物的键能和=(945+498)kJ/mol-2×630kJ/mol=+183kJ/mol,所以N2和O2反应生成NO的热化学反应方程式为N2(g)+O2(g)=2NO(g)△H=+183kJ•mol-1,该反应在常温下非自发进行,则△G=△H-T△S在低温时△G>0,所以△S>0,
故答案为:+183 kJ/mol,>;
(2)①2NO2(g)+NaCl(s)?NaNO3(s)+ClNO(g),△H1<0 (Ⅰ),平衡常数K1=$\frac{[ClNO]}{[N{O}_{2}]^{2}}$,
2NO(g)+Cl2(g)?2ClNO(g),△H2<0 (Ⅱ),平衡常数K2 =$\frac{[ClNO]^{2}}{[NO]^{2}[C{l}_{2}]}$,
4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=$\frac{[C{l}_{2}][NO]^{2}}{[N{O}_{2}]^{4}}$,计算得到K=$\frac{{{K}_{1}}^{2}}{{K}_{2}}$,
故答案为:$\frac{{{K}_{1}}^{2}}{{K}_{2}}$;
②在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(Ⅱ)达到平衡,测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,物质的量为7.5×10-3mol•L-1•min-1×10min×2L=0.15mol,
2NO(g)+Cl2(g)?2ClNO(g),
起始量(mol) 0.2 0.1 0
变化量(mol) 0.15 0.075 0.15
平衡量(mol) 0.05 0.025 0.15
则平衡后n(Cl2)=0.025mol,
NO的转化率α1=$\frac{0.15mol}{0.2mol}$×100%=75%;
故答案为:0.025;75%;
③其他条件保持不变,反应(Ⅱ)在恒压条件下进行,随反应进行,气体体积减小,为保持恒压所以容器体积减小,压强比恒容容器大,平衡正向进行,平衡时NO的转化率α2 增大;平衡常数随温度变化,不随浓度、压强变化,若要使K2减小,平衡逆向进行,反应是放热反应,依据平衡移动原理应升高温度,平衡逆向进行,
故答案为:>;不变;升高温度;
(3)合成氨的反应是放热反应,反应达到一定温度才可以发生反应,开始反应,氨气物质的量增大,达到平衡状态,继续升温,平衡逆向进行,氨气物质的量减小,画出的图象为 ,故答案为;
,故答案为; .
.
点评 本题涉及化学反应的能量变化以及化学平衡等知识,化学平衡常数的计算,影响化学平衡的因素分析应用判断,属于综合知识的考查,掌握基础是关键,题目难度中等.

 出彩同步大试卷系列答案
出彩同步大试卷系列答案
| A. | 充电时阴极的电极反应是V3++e-=V2+ | |
| B. | 放电时,VO2+作氧化剂,在正极被还原,V2+做还原剂,在负极被被氧化 | |
| C. | 若离子交换膜为质子交换膜,充电时当有1mol e-发生转移时,左槽电解液的H+的物质的量增加了1mol | |
| D. | 若离子交换膜为阴离子交换膜,放电时阴离子由左罐移向右罐 |
| A. | CO32- | B. | SO42- | C. | Cl- | D. | Na+ |
| A. | Na2CO3溶液中通入少量SO2:SO2+H2O+2CO32-═SO32-+2HCO3- | |
| B. | 漂白粉中滴加浓盐酸加热制取氯气:ClO-+Cl-+2H+ $\frac{\underline{\;\;△\;\;}}{\;}$ Cl2+H2O | |
| C. | 将0.1mol•L-1的NH4Al(SO4)2溶液与0.2mol•L-1的Ba(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═AlO2-↓+2BaSO4↓+2H2O | |
| D. | 含0.4molFeI2的溶液中通入0.3mol氯气:4Fe2++2I-+3Cl2═4Fe3++I2+6Cl- |
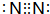 .
.