题目内容
下列有关阿伏加德罗常数(NA)的说法错误的是( )
| A、常温常压下28克N2所含的原子数目为2NA |
| B、标准状况下0.5molH2O含有的原子数目为1.5NA |
| C、任何条件下0.5mol氨气分子的分子数一定是0.5NA |
| D、49克H2SO4中含有的原子数目为1.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、氮气为双原子分子,依据质量求出物质的量和原子数;
B、根据1mol水含3mol原子来计算;
C、根据N=nNA来计算;
D、根据硫酸的物质的量n=
,而1molH2SO4中含7mol原子.
B、根据1mol水含3mol原子来计算;
C、根据N=nNA来计算;
D、根据硫酸的物质的量n=
| m |
| M |
解答:
解:A、氮气为双原子分子,28克氮气的物质的量为n=
=
1mol,则氮原子为2mol,所以所含的原子数目为2NA,故A正确;
B、1mol水含3mol原子,故0.5mol水中含1.5mol原子,故B正确;
C、0.5mol氨气中的分子个数N=nNA=0.5mol×NA=0.5NA,无状态无关,故C正确;
D、49g硫酸的物质的量n=
=
=0.5mol,而1molH2SO4中含7mol原子,故0.5mol硫酸含3.5mol,故D错误.
故选D.
| m |
| M |
| 28g |
| 28g/mol |
B、1mol水含3mol原子,故0.5mol水中含1.5mol原子,故B正确;
C、0.5mol氨气中的分子个数N=nNA=0.5mol×NA=0.5NA,无状态无关,故C正确;
D、49g硫酸的物质的量n=
| m |
| M |
| 49g |
| 98g/mol |
故选D.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
下列物质中既能跟稀H2SO4反应,又能跟氢氧化钠溶液反应的是( )
①NaHCO3②Al2O3③Al(OH)3 ④Al.
①NaHCO3②Al2O3③Al(OH)3 ④Al.
| A、③④ | B、②③④ |
| C、①③④ | D、①②③④ |
下列说法正确的是( )
| A、二氧化硫具有漂白性,所以可以使溴水褪色 |
| B、硫在少量氧气中燃烧生成二氧化硫,在过量氧气中燃烧生成三氧化硫 |
| C、雷雨天氮元素可以进行下列转化:N2→NO→NO2→HNO3 |
| D、氮气的化学性质非常稳定,不支持任何物质的燃烧 |
在某无色透明的酸性溶液中,能共存的离子组是( )
| A、NH4+、NO3-、Al3+、I- |
| B、Na+、Al3+、K+、NO3- |
| C、Cu2+、K+、SO42-、Na+ |
| D、K+、SO42-、HCO3-、NO3- |
下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A、1.8g NH4+ 所含原子数为0.1NA |
| B、通常状况下,NA个CO2分子占有的体积为22.4 L |
| C、物质的量浓度为0.5mol/L的BaCl2溶液中,含有Cl- 个数为NA |
| D、1 mol?L-1的CaCl2溶液中,Cl-的物质的量浓度为2 mol?L-1 |
能正确表示下列化学反应的离子方程式的是( )
| A、氢氧化钡溶液与稀硫酸的反应 OH-+H+=H2O |
| B、氧化钙与稀盐酸反应CaO+2H+=Ca2++H2O |
| C、铁片插入硝酸银溶液中Fe+Ag+=Fe2++Ag |
| D、碳酸钙溶于稀硝酸中 CO32++2H+=CO2↑+H2O |
下列化学用语只能用来表示一种微粒的是( )
A、 |
B、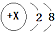 |
| C、CH4O |
| D、C |