题目内容
8.下列物质中:①Na ②蔗糖 ③CO ④AgCl ⑤CO2⑥NaCl溶液 ⑦NH3⑧H2S ⑨H2SO4⑩Ba(OH)2属于电解质的是④⑧⑨⑩;属于强电解质的是④⑨⑩;
属于非电解质的是②③⑤⑦;能导电的是①⑥;
属于酸性氧化物的是⑤.
分析 电解质和非电解质都必须是化合物;电解质在熔融状态或水溶液中能导电的化合物,非电解质是在熔融状态和水溶液中都不能导电的化合物,金属单质能导电;电解质在熔融状态或水溶液中能导电;强电解质是指在水溶液中完全电离的化合物;能和碱反应生成盐和水的氧化物是酸性氧化物,据此即可解答.
解答 解:④⑧⑨⑩是在熔融状态或水溶液中能导电的化合物,属于电解质;④⑨⑩是在水溶液中完全电离的化合物,属于强电解质;②③⑤⑦是在熔融状态和水溶液中都不能导电的化合物,属于非电解质;能导电的是①⑥;⑤能和碱反应生成盐和水的氧化物,属于酸性氧化物.
故答案为:④⑧⑨⑩;④⑨⑩;②③⑤⑦;①⑥;⑤.
点评 本题考查了电解质与非电解质、物质的导电性判断,题目难度不大,注意明确电解质与非电解质的本质区别,明确溶液导电性原因是关键.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
11.下列说法正确的是( )
| A. | HOCH2COOH既可以发生取代反应又可以发生缩聚反应 | |
| B. | 蔗糖、纤维素的水解过程都是高分子转化为小分子的过程 | |
| C. | 甲烷、甲醛、甲酸都不存在同分异构体,则甲醚(CH3OCH3)也无同分异构体 | |
| D. | 按系统命名法,化合物 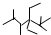 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 |
12.常温下,将某可溶性一元碱X0H和盐酸等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明XOH是强碱还是弱碱a=7为强碱,a<7为弱碱.
(2)考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2否(选填“是”或“否”).混合液中离子浓度c(Cl-)与 c(X+)的大小关系是c(Cl-)=c(X+).
(3)丙组实验结果分析,XOH是弱碱(选填“强”或“弱”).该混合溶液中离子浓度由大到小的顺序是
(Cl-)>c(X+)>c(H+)>c(OH-).
(4)若甲组实验中a=5,则该混合溶液中:
c(Cl-)-c(X+)=10-5-10-9mol•L-1; c(H+)-c(XOH)=10-9mol•L-1.
| 实验编号 | XOH物质的量浓度(mol•L-1) | 盐酸物质的量浓度(mol•L-1) | 混合溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | b | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH<7 |
(2)考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2否(选填“是”或“否”).混合液中离子浓度c(Cl-)与 c(X+)的大小关系是c(Cl-)=c(X+).
(3)丙组实验结果分析,XOH是弱碱(选填“强”或“弱”).该混合溶液中离子浓度由大到小的顺序是
(Cl-)>c(X+)>c(H+)>c(OH-).
(4)若甲组实验中a=5,则该混合溶液中:
c(Cl-)-c(X+)=10-5-10-9mol•L-1; c(H+)-c(XOH)=10-9mol•L-1.
16.下列现象不能用胶体的性质解释的是( )
①用氯气对自来水消毒 ②用石膏或盐卤点制豆腐 ③清晨的阳光穿过茂密的林木枝叶产生美丽的光圈 ④在NaCl溶液中滴入AgNO3溶液产生沉淀 ⑤长江水在入海口形成三角洲.
①用氯气对自来水消毒 ②用石膏或盐卤点制豆腐 ③清晨的阳光穿过茂密的林木枝叶产生美丽的光圈 ④在NaCl溶液中滴入AgNO3溶液产生沉淀 ⑤长江水在入海口形成三角洲.
| A. | ①② | B. | ②③⑤ | C. | ①④ | D. | 只有④ |
3.下列现象不能用胶体知识进行解释的是( )
| A. | 向FeCl3饱和溶液中滴加NaOH溶液形成红褐色的分散系 | |
| B. | 一支钢笔使用两种不同牌子的蓝黑墨水,易出现堵塞 | |
| C. | 在河水与海水的交界处,易有三角洲形成 | |
| D. | 水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷 |
17.下列实验可行的是( )
| A. | 苯、CCl4、酒精可用来萃取溴水中的溴 | |
| B. | 用激光笔鉴别Fe(OH)3胶体和FeCl3溶液 | |
| C. | 加入盐酸以除去硫酸钠中的少量碳酸钠杂质 | |
| D. | 在容量瓶中加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸 |
18.铁及其化合物在日常生活、生产中应用广泛.
(1)在某温度下,Ksp(FeS)=8.1×10-17,FeS饱和溶液中c(H+)与c(S2-)之间存在关系:c2(H+)•c(S2-)=1.0×10-22,为了使溶液里c(Fe2+)达到1mol•L-1,现将适量FeS投入其饱和溶液中,应调节溶液中的pH约为B(填字母).
A.2 B.3 C.4 D.5
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆.以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
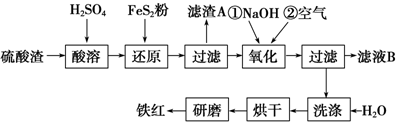
①酸溶过程中Fe2O3发生反应的离子方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
“滤渣A”主要成分的化学式为SiO2.
②还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4.
请完成该反应的离子方程式:1FeS2+14Fe3++8H2O═15Fe2++2SO${\;}_{4}^{2-}$+16H+
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为4Fe2++O2+2H2O+8OH-=4Fe(OH)3↓.
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是3.2~3.8.
如果pH过大,可能引起的后果是Al3+、Mg2+形成沉淀,使制得的铁红不纯(几种离子沉淀的pH见上表).
⑤滤液B可以回收的物质有ABD(填序号).
A.Na2SO4 B.Al2(SO4)3 C.Na2SiO3 D.MgSO4.
(1)在某温度下,Ksp(FeS)=8.1×10-17,FeS饱和溶液中c(H+)与c(S2-)之间存在关系:c2(H+)•c(S2-)=1.0×10-22,为了使溶液里c(Fe2+)达到1mol•L-1,现将适量FeS投入其饱和溶液中,应调节溶液中的pH约为B(填字母).
A.2 B.3 C.4 D.5
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆.以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:

①酸溶过程中Fe2O3发生反应的离子方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
“滤渣A”主要成分的化学式为SiO2.
②还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4.
请完成该反应的离子方程式:1FeS2+14Fe3++8H2O═15Fe2++2SO${\;}_{4}^{2-}$+16H+
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为4Fe2++O2+2H2O+8OH-=4Fe(OH)3↓.
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是3.2~3.8.
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
⑤滤液B可以回收的物质有ABD(填序号).
A.Na2SO4 B.Al2(SO4)3 C.Na2SiO3 D.MgSO4.
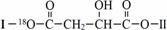 (其中Ⅰ、Ⅱ为未知部分的结构).下列是X发生反应的转化关系图及E的信息.
(其中Ⅰ、Ⅱ为未知部分的结构).下列是X发生反应的转化关系图及E的信息.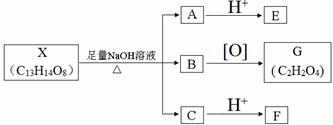
 .
.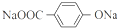 ;X的结构简式是
;X的结构简式是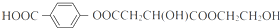 .
.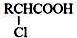 ;RCH2Br$→_{②H_{2}O/H+}^{①NaCN}$RCH2COOH
;RCH2Br$→_{②H_{2}O/H+}^{①NaCN}$RCH2COOH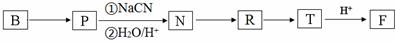
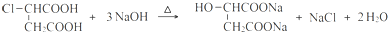 .
.