题目内容
有一固体粉末,可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验.
(1)将该粉末溶于水得无色溶液和白色沉淀;
(2)在滤出的沉淀中加入稀硝酸,部分沉淀溶解,同时产生无色气体;
(3)取滤液做焰色反应,可以看到黄色火焰,透过蓝色钴玻璃片,观察不到紫色火焰.由上述现象可推断( )
(1)将该粉末溶于水得无色溶液和白色沉淀;
(2)在滤出的沉淀中加入稀硝酸,部分沉淀溶解,同时产生无色气体;
(3)取滤液做焰色反应,可以看到黄色火焰,透过蓝色钴玻璃片,观察不到紫色火焰.由上述现象可推断( )
| A、可能有Na2CO3 |
| B、一定有Na2SO4 |
| C、一定无NaCl |
| D、一定有K2SO4 |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:由(1)将该粉末溶于水得无色溶液和白色沉淀,可判断一定无CuCl2,一定有Ba(NO3)2,因为只有钡离子才可以形成沉淀,同时可能含碳酸根的化合物或含硫酸根离子的化合物;
由(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体,说明沉淀一定有硫酸钡和碳酸钡;
由(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰,说明一定有钠离子一定无钾离子,所以原混合物中一定含有Na2CO3和Na2SO4,一定不含有K2CO3和K2SO4,以此来解答.
由(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体,说明沉淀一定有硫酸钡和碳酸钡;
由(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰,说明一定有钠离子一定无钾离子,所以原混合物中一定含有Na2CO3和Na2SO4,一定不含有K2CO3和K2SO4,以此来解答.
解答:
解:由(1)将该粉末溶于水得无色溶液和白色沉淀,可判断一定无CuCl2,一定有Ba(NO3)2,因为只有钡离子才可以形成沉淀,同时可能含碳酸根的化合物或含硫酸根离子的化合物;
由(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体,说明沉淀一定有硫酸钡和碳酸钡,反应为Ba2++SO42-=BaSO4↓,Ba2++CO32-=BaCO3↓,BaCO3+2H+=Ba2++CO2↑+H2O;
由③取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰,说明一定有钠离子一定无钾离子,所以原混合物中一定含有Na2CO3和Na2SO4,一定不含有K2CO3和K2SO4;
由上述分析可知,原混合物中一定含有Na2CO3、Na2SO4、Ba(NO3)2,一定不含有CuCl2、K2CO3、K2SO4,可能含有NaCl,
故选B.
由(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体,说明沉淀一定有硫酸钡和碳酸钡,反应为Ba2++SO42-=BaSO4↓,Ba2++CO32-=BaCO3↓,BaCO3+2H+=Ba2++CO2↑+H2O;
由③取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰,说明一定有钠离子一定无钾离子,所以原混合物中一定含有Na2CO3和Na2SO4,一定不含有K2CO3和K2SO4;
由上述分析可知,原混合物中一定含有Na2CO3、Na2SO4、Ba(NO3)2,一定不含有CuCl2、K2CO3、K2SO4,可能含有NaCl,
故选B.
点评:本题考查物质检验和鉴别,为高频考点,把握物质的性质及实验现象为解答的关键,侧重分析推断能力及知识综合应用能力的考查,注意常见离子的检验方法,题目难度不大.

练习册系列答案
相关题目
在水中加入等物质的量的Ag+、Ba2+、SO42-、NO3-、Cl-、Na+,用惰性材料作电极进行电解,通电片刻后停止,下列说法不正确的是( )
| A、电解的实质是:阳极:2Cl--2e-=Cl2↑;阴极:Ag+e-=Ag |
| B、电解的实质是:阳极:4OH--4e-=2H2O+O2↑;阴极:2H++2e-=H2↑ |
| C、要恢复成电解前的溶液可以加水 |
| D、电解产物中氧化产物和还原产物的物质的量之比为1:2 |
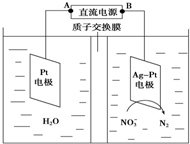 目前废水处理中的除氮技术,通常是把水中的氨氮污染物先降解为NO3- 或NO2-,然后再用电解的方法除去NO3-和NO2-,如图是电化学降解硝酸盐的原理,关于该原理的说法正确的是( )
目前废水处理中的除氮技术,通常是把水中的氨氮污染物先降解为NO3- 或NO2-,然后再用电解的方法除去NO3-和NO2-,如图是电化学降解硝酸盐的原理,关于该原理的说法正确的是( )| A、Pt电极为阴极 |
| B、电解过程中H+向正极移动 |
| C、理论上电解过程中阴、阳两极产生的气体在相同条件下体积比为2:5 |
| D、电解过程中Pt电极附近溶液的pH增大 |
可以用来鉴别Cl-、Br-、I-离子的是( )
| A、AgNO3溶液和稀硝酸 |
| B、观察它们的颜色 |
| C、用焰色反应进行实验 |
| D、分别向里滴加氯水 |
下面的说法不正确的是( )
| A、用纯碱溶液清洗油污时,加热可以增强其去污能力 |
| B、区别NaCl、NH4Cl、Na2CO3三种无色透明溶液用pH试纸鉴别,pH=7的是NaCl溶液,pH<7的是NH4Cl溶液,pH>7的是Na2CO3溶液 |
| C、用氯化铝(AlCl3 )溶液和硫化钠(Na2S)溶液混合制取硫化铝(Al2S3)溶液 |
| D、常温下相同物质的量浓度碳酸钠溶液和醋酸钠溶液,其pH值前者大于后者 |
食盐、食醋、纯碱均为家庭厨房中常用的物质.利用这些物质不能完成的实验是( )
| A、鉴别食盐和纯碱 |
| B、验证蛋壳的主要成分为CaCO3 |
| C、除去热水瓶内壁上的水垢 |
| D、检验自来水中是否含有Cl- |
下列检验某未知溶液中是否含有SO42-的操作中,最合理的是( )
| A、先加HCl酸化,再加BaCl2溶液 |
| B、加入HCl酸化了的BaCl2溶液 |
| C、先加HNO3酸化,再加Ba(NO3)2溶液 |
| D、加入HNO3酸化了的Ba(NO3)2溶液 |
200℃时,11.6g CO2和水蒸气的混合气与过量的Na2O2充分反应后,固体质量增加了3.6g,再将反应后剩余固体冷却后加入含有Na+、HCO3-、SO32-、CO32-等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是( )
| A、原混合气体的平均摩尔质量为23.2g/mol |
| B、混合气体与Na2O2反应过程中电子转移的物质的量为0.25mol |
| C、溶液中SO32-的物质的量浓度基本保持不变 |
| D、溶液中HCO3-的物质的量浓度减小,CO32-的物质的量浓度增大,但是加入“剩余固体”充分反应后溶液中HCO3-和CO32-的物质的量浓度之和与加入“剩余固体”前基本保持不变 |