题目内容
有X、Y、Z、V、W五种短周期元素,已知:
①Z+、V3+均与W的气态氢化物分子具有相同的电子数;X2-、Y-与Y的气态氢化物分子具有相同的电子数:
②X单质在空气中燃烧产生气体R;
③Y的气态氢化物与W的气态氢化物相遇时有白烟生成.
请回答:
(1)X2-的结构示意图为 .
(2)元素W在元素周期表中的位置是 .
(3)元素Z的单质在空气中燃烧产物的化学式为 .
(4)元素Z的最高价氧化物的水化物是一种强碱,写出元素V的单质与该强碱溶液反应的离子方程式: .
(5)向Y单质的水溶液中通入过量气体R反应的离子方程式为: .
①Z+、V3+均与W的气态氢化物分子具有相同的电子数;X2-、Y-与Y的气态氢化物分子具有相同的电子数:
②X单质在空气中燃烧产生气体R;
③Y的气态氢化物与W的气态氢化物相遇时有白烟生成.
请回答:
(1)X2-的结构示意图为
(2)元素W在元素周期表中的位置是
(3)元素Z的单质在空气中燃烧产物的化学式为
(4)元素Z的最高价氧化物的水化物是一种强碱,写出元素V的单质与该强碱溶液反应的离子方程式:
(5)向Y单质的水溶液中通入过量气体R反应的离子方程式为:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:Y的气态氢化物与W的气态氢化物相遇有白烟生成,则一种是氨气、一种是HCl,Y能形成-1价阴离子,则Y是Cl元素、W是N元素;Z+、V 3+均与W的气态氢化物分子具有相同的电子式,则Z是Na元素、V是Al元素,X 2-、Y-与Y的气态氢化物分子具有相同的电子数,则X是S元素,S在空气中燃烧产生气体SO2,所以R为SO2,
(1)S2-离子核外有3个电子层、最外层电子数是8,据此书写其离子结构示意图;
(2)元素W为N,主族元素原子核外电子层数与其周期数相等,最外层电子数与其族序数相等;
(3)元素Z为Na,Na在空气中燃烧生成淡黄色的过氧化钠;
(4)元素Z为Na元素,Na的最高价氧化物的水化物是一种强碱,为NaOH,元素V的单质为Al,Al和强碱NaOH溶液反应生成四羟基合铝酸钠和氢气和氢气;
(5)Y为Cl元素,R为SO2,氯气和二氧化硫在水溶液里发生氧化还原反应生成硫酸和盐酸.
(1)S2-离子核外有3个电子层、最外层电子数是8,据此书写其离子结构示意图;
(2)元素W为N,主族元素原子核外电子层数与其周期数相等,最外层电子数与其族序数相等;
(3)元素Z为Na,Na在空气中燃烧生成淡黄色的过氧化钠;
(4)元素Z为Na元素,Na的最高价氧化物的水化物是一种强碱,为NaOH,元素V的单质为Al,Al和强碱NaOH溶液反应生成四羟基合铝酸钠和氢气和氢气;
(5)Y为Cl元素,R为SO2,氯气和二氧化硫在水溶液里发生氧化还原反应生成硫酸和盐酸.
解答:
解:Y的气态氢化物与W的气态氢化物相遇有白烟生成,则一种是氨气、一种是HCl,Y能形成-1价阴离子,则Y是Cl元素、W是N元素;Z+、V 3+均与W的气态氢化物分子具有相同的电子式,则Z是Na元素、V是Al元素,X 2-、Y-与Y的气态氢化物分子具有相同的电子数,则X是S元素,S在空气中燃烧产生气体SO2,所以R为SO2,
(1)S2-离子核外有3个电子层、最外层电子数是8,所以硫离子结构示意图为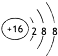 ,故答案为:
,故答案为: ;
;
(2)元素W为N,主族元素原子核外电子层数与其周期数相等,最外层电子数与其族序数相等,N原子核外有2个电子层、最外层电子数是5,所以N元素位于第二周期第VA族,故答案为:第二周期第VA族;
(3)元素Z为Na,Na在空气中燃烧生成淡黄色的Na2O2,故答案为:Na2O2;
(4)元素Z为Na元素,Na的最高价氧化物的水化物是一种强碱,为NaOH,元素V的单质为Al,Al和强碱NaOH溶液反应生成四羟基合铝酸钠和氢气,离子方程式为2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑,故答案为:2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑;
(5)Y为Cl元素,R为SO2,氯气和二氧化硫在水溶液里发生氧化还原反应生成硫酸和盐酸,离子方程式为Cl2+SO2+2H2O=4H++SO42-+2Cl-,故答案为:Cl2+SO2+2H2O=4H++SO42-+2Cl-.
(1)S2-离子核外有3个电子层、最外层电子数是8,所以硫离子结构示意图为
 ,故答案为:
,故答案为: ;
;(2)元素W为N,主族元素原子核外电子层数与其周期数相等,最外层电子数与其族序数相等,N原子核外有2个电子层、最外层电子数是5,所以N元素位于第二周期第VA族,故答案为:第二周期第VA族;
(3)元素Z为Na,Na在空气中燃烧生成淡黄色的Na2O2,故答案为:Na2O2;
(4)元素Z为Na元素,Na的最高价氧化物的水化物是一种强碱,为NaOH,元素V的单质为Al,Al和强碱NaOH溶液反应生成四羟基合铝酸钠和氢气,离子方程式为2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑,故答案为:2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑;
(5)Y为Cl元素,R为SO2,氯气和二氧化硫在水溶液里发生氧化还原反应生成硫酸和盐酸,离子方程式为Cl2+SO2+2H2O=4H++SO42-+2Cl-,故答案为:Cl2+SO2+2H2O=4H++SO42-+2Cl-.
点评:本题考查位置结构性质的相互关系及应用,涉及离子方程式的书写、氧化还原反应、原子结构等知识点,侧重考查基本理论、化学用语,明确离子方程式书写规则及物质性质、原子结构即可解答,熟练掌握元素化合物知识,题目难度不大.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
下列说法中不正确的是( )
| A、溶解度:Na2CO3大于NaHCO3 |
| B、稳定性:Na2CO3大于NaHCO3 |
| C、与酸反应剧烈程度:NaHCO3大于Na2CO3 |
| D、石灰水可与Na2CO3反应而不与NaHCO3反应 |
下列表示式正确的是( )
A、甲烷的球棍模型: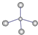 |
B、CO2分子的比例模型: |
| C、淀粉分子的最简式:CH2O |
| D、乙烯的结构简式 CH2=CH2 |
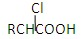
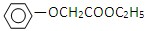 .
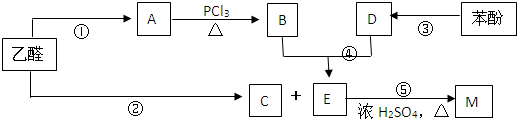
.
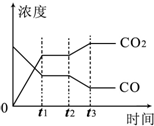 对于反应CO(g)+H2O(g)?H2(g)+CO2(g)
对于反应CO(g)+H2O(g)?H2(g)+CO2(g)