题目内容
6.关于铝原子或铝离子的结构错误的是( )| A. | 原子的最外层电子数等于电子层数 | |
| B. | 反应中可失去三个电子,比镁、钠还原性弱 | |
| C. | 失去电子的铝离子半径比铝原子小 | |
| D. | 铝离子比镁离子、钠离子的半径大 |
分析 A.Al原子最外层含有3个电子、3个电子层;
B.Al最外层含有3个电子,反应中可失去3个电子,Al的活泼性比Mg、Na弱;
C.铝离子含有2个电子层,铝原子含有个电子层,电子层越多,粒子半径越大;
D.电子层相同时,离子的核电荷数越大,离子半径越小.
解答 解:A.Al原子的最外层电子数、电子层数都是3,故A正确;
B.Al原子最外层电子数为3,可以失去3个电子,金属铝的还原性小于Mg、Na,故B错误;
C.铝原子比铝离子多1个电子层,则失去电子的铝离子半径比铝原子小,故C正确;
D.铝离子、镁离子、钠离子都含有2个电子层,铝的核电荷数大于Na和Mg,则铝离子比镁离子、钠离子的半径小,故D错误;
故选C.
点评 本题考查了铝的性质,题目难度不大,明确常见元素及其化合物性质为解答关键,注意掌握Al的结构与性质,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
16.下列说法不正确的是( )
| A. | 向Na2CO3溶液中逐滴加入HCl,直到不再生成CO2气体为止,在此过程中,溶液中HCO3-的浓度变化是先变大后变小(溶液体积变化均忽略不计) | |
| B. | 向NaHCO3溶液中加入Ba(OH)2固体,CO32-的浓度变化是先变大后变小(溶液体积变化均忽略不计) | |
| C. | 有含0.2molNa2CO3和含0.3molHCl的两种溶液:①将Na2CO3溶液逐滴滴入HCl溶液中;②将HCl溶液逐滴滴入Na2CO3溶液中.①②两种操作生成CO2的体积之比为3:2 | |
| D. | 将等质量的Na2O和Na2O2样品分别放入等量的水中,所得溶液的质量分数分别为a%和b%,则a、b的关系是a=b |
17.化学与生产、生活、社会密切相关,下列有关说法正确的是( )
| A. | 光导纤维在信息领域应用越来越广泛,其主要成分是硅单质 | |
| B. | “地沟油”禁止食用,但可以用来制肥皂 | |
| C. | 明矾常用于水体杀菌消毒 | |
| D. | 中秋将至,为防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰 |
1.下列叙述不正确的是( )
| A. | 化学反应释放或吸收能量的多少与发生反应的反应物的物质的量有关 | |
| B. | 人们可以利用氧化还原反应设计原电池以获取电能 | |
| C. | 人们可以利用C2H2(乙炔)与O2的化学反应获取热能或电能或光能 | |
| D. | MnO4-+5e-+8H+═Mn2++4H2O可能是某原电池里的负极反应 |
4.下列物质中,含有离子键的是( )
| A. | H2 | B. | HCl | C. | NaCl | D. | CO2 |
11.下列电子排布式或轨道表示式正确的是( )
①C原子的轨道表示式: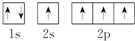
②Cr原子的电子排布式:1s22s22p63s23p63d44s2
③O原子的轨道表示式: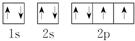
④Br原子的外围电子排布式:3d104s24p5
⑤B原子的轨道表示式: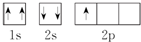
①C原子的轨道表示式:

②Cr原子的电子排布式:1s22s22p63s23p63d44s2
③O原子的轨道表示式:

④Br原子的外围电子排布式:3d104s24p5
⑤B原子的轨道表示式:

| A. | ①②③ | B. | ②③④ | C. | ①②④⑤ | D. | 只有③ |
8.下列说法中,正确的是( )
| A. | RCOOH与R′OH发生酯化反应时生成R′OOCR | |
| B. | 能与NaOH溶液反应,分子式为C2H4O2的有机物一定是羧酸 | |
| C. | 甲酸乙酯、乙酸甲酯、丙酸互为同分异构体 | |
| D. | 甲醛与乙酸乙酯的最简式相同 |