题目内容
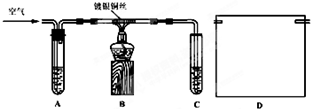
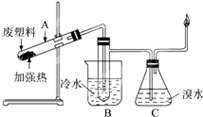 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热某废塑料得到的产物如下表
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热某废塑料得到的产物如下表| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
(2)锥形瓶C中观察到的现象
(3)写出C中逸出的气体在工业上的两种用途
考点:常用合成高分子材料的化学成分及其性能
专题:有机化合物的获得与应用
分析:(1)先找出能使酸性高锰酸钾溶液褪色的物质,再找出物质的一氯代物的种类;B中收集到得有机物为苯和甲苯,二者与溴水混合发生萃取;
(2)产物中的乙烯、丙烯能够与溴水发生加成反应;经溴水充分吸收,剩余气体为氢气和甲烷,根据二者的含量求算;
(3)C中最后逸出的气体是甲烷和氢气,根据所学知识找出二者用途.
(2)产物中的乙烯、丙烯能够与溴水发生加成反应;经溴水充分吸收,剩余气体为氢气和甲烷,根据二者的含量求算;
(3)C中最后逸出的气体是甲烷和氢气,根据所学知识找出二者用途.
解答:
解:(1)试管B中含有苯和甲苯,苯不能使高锰酸钾褪色,甲苯可以使高锰酸钾褪色,一氯甲苯的同分异构体有:
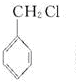
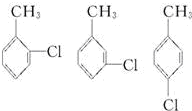 ,总计4种;B中收集到得有机物为苯和甲苯,二者与溴水混合发生萃取,溴溶在苯和甲苯的混合物中在水的上层,所以观察到得现象为液体分层,下层无色,上层为橙色;
,总计4种;B中收集到得有机物为苯和甲苯,二者与溴水混合发生萃取,溴溶在苯和甲苯的混合物中在水的上层,所以观察到得现象为液体分层,下层无色,上层为橙色;
故答案为:4;液体分层,下层无色,上层为橙色;
(2)产物中的乙烯、丙烯分子中含有碳碳双键,能够与溴水发生反应,溴水褪色;经溴水充分吸收,剩余气体为氢气和甲烷,已知氢气的质量分数为12%,甲烷的质量分数为24%,令质量为ag,则氢气的物质的量为
,甲烷的物质的量为
,则平均相对分子质量=
=4.8;
故答案为:棕黄色溶液变无色或褪色;4.8;
(3)最后得到的气体是甲烷和氢气,氢气可以用于合成氨工业,甲烷可以做燃料,
故答案为:合成氨原料;作燃料或有机化工原料(或其他合理答案).

 ,总计4种;B中收集到得有机物为苯和甲苯,二者与溴水混合发生萃取,溴溶在苯和甲苯的混合物中在水的上层,所以观察到得现象为液体分层,下层无色,上层为橙色;
,总计4种;B中收集到得有机物为苯和甲苯,二者与溴水混合发生萃取,溴溶在苯和甲苯的混合物中在水的上层,所以观察到得现象为液体分层,下层无色,上层为橙色;故答案为:4;液体分层,下层无色,上层为橙色;
(2)产物中的乙烯、丙烯分子中含有碳碳双键,能够与溴水发生反应,溴水褪色;经溴水充分吸收,剩余气体为氢气和甲烷,已知氢气的质量分数为12%,甲烷的质量分数为24%,令质量为ag,则氢气的物质的量为
| 12%a |
| 2 |
| 24%a |
| 16 |
| 12%a+24%a | ||
6%a+
|
故答案为:棕黄色溶液变无色或褪色;4.8;
(3)最后得到的气体是甲烷和氢气,氢气可以用于合成氨工业,甲烷可以做燃料,
故答案为:合成氨原料;作燃料或有机化工原料(或其他合理答案).
点评:本题考查了烯烃和苯及其同系物的性质,是一道实验综合题,涉及的知识点较多,准确判断甲苯的4种一氯代物是解答该题的易错点,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
100℃时,两种气态烃以任意比混合,1L混合烃与9L O2混合,充分燃烧后恢复到原状态,所得气体体积仍为10L.下列各组混合烃不符合此条件的是( )
| A、CH4和C2H4 |
| B、CH4和C3H4 |
| C、C2H2和C3H6 |
| D、C2H4和C3H4 |
下列物质的性质、用途正确的是( )
| A、浓硫酸、浓硝酸都具有强氧化性,不能盛放在金属容器中 |
| B、Na2SiO3是制备硅胶和木材防火剂的原料 |
| C、食盐可作调味剂,不可作防腐剂 |
| D、合金的硬度大,熔点也高 |
下列说法正确的是( )
| A、将pH=5的硫酸溶液稀释500倍溶液中c(SO42-):c(H+)≈1:10 |
| B、常温下,将pH=5的醋酸溶液稀释100倍后溶液pH=7 |
| C、常温下,将pH=9的氢氧化钠溶液稀释100倍后溶液pH=7 |
| D、常温下,将0.01mol?L-1的硫酸溶液稀释100倍后溶液pH=4 |
下列下列化学用语正确的是( )
| A、三氯化铁溶液中加入铁粉Fe3++Fe═2Fe2+ |
B、过氧化钠电子式: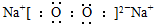 |
C、Na+结构简图: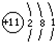 |
| D、少量氯气通入溴化亚铁溶液中2FeBr2+3Cl2═2FeCl3+2 Br2 |
干燥剂的干燥性能可用干燥效率(1m3空气中实际余留水蒸气的质量)来衡量.某些干燥剂的干燥效率数据如下分析以上数据,下列有关叙述错误的是.( )
| 物质 | 干燥效率 | 物质 | 干燥效率 |
| MgO | 0.008 | ZnCl2 | 0.8 |
| CaO | 0.2 | ZnBr2 | 1.1 |
| A、MgO的干燥性能比CaO好 |
| B、干燥效率可能与干燥剂的阴、阳离子的半径大小有关 |
| C、MgCl2可能是比CaCl2更好的干燥剂 |
| D、上述干燥剂中阳离子对干燥剂性能的影响比阴离子小 |
 已知:用惰性电极电解某盐X的溶液,发生的反应为:X+H2O
已知:用惰性电极电解某盐X的溶液,发生的反应为:X+H2O