题目内容
13.将等质量的Zn粉分别投入:a:10mL 0.1mol•L-1 HCl和b:10mL 0.1mol•L-1醋酸中.
①若Zn不足量,则反应速率a>b.(填“>”、“=”或“<”,下同)
②若Zn过量,产生H2的量a=b.
分析 物质的量浓度相等的盐酸和醋酸,醋酸中氢离子浓度小于盐酸,
①若Zn不足量,酸有剩余,相同浓度的醋酸和盐酸中,反应过程中醋酸中氢离子浓度小于盐酸,氢离子浓度越大,反应速率越大;
②若Zn过量,产生H2的量与酸的物质的量成正比.
解答 解:物质的量浓度相等的盐酸和醋酸,醋酸中氢离子浓度小于盐酸,
①若Zn不足量,酸有剩余,相同浓度的醋酸和盐酸中,盐酸中氢离子浓度大于醋酸,所以盐酸反应速率大于醋酸,故答案为:>;
②若Zn过量,产生H2的量与酸的物质的量成正比,醋酸和盐酸都是一元酸,且体积、浓度相等,则其物质的量硝酸,所以生成氢气的物质的量相等,故答案为:=.
点评 本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,知道反应速率与离子浓度成正比、与电解质强弱无关,为易错点.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
4.砹是原子序数最大的卤族元素、根据卤素性质的递变规律,对砹及其化合物的叙述,正确的是( )
| A. | 与H2化合能力:At2>I2 | B. | 砹在常温下为白色固体 | ||
| C. | 砹原子的最外电子层上有7个电子 | D. | 砹能从NaCl溶液中置换出氯单质 |
1.如表实验操作能达到相应目的是( )
| 编号 | 实验操作 | 目的 |
| A | 取4gNaOH固体溶于100mL水中 | 配制0.1mol•L-1NaOH溶液 |
| B | 向沸水中逐滴加入1-2mLFeCl3饱和溶液,搅拌并继续煮沸到变成红褐色 | 制备Fe(OH)3胶体 |
| C | 测定等物质的量浓度的盐酸、硝酸的pH | 比较Cl、N的非金属性 |
| D | 用MgCl2、AlCl3溶液做导电性试验 | 证明两者是离子化合物还是共价化合物 |
| A. | A | B. | B | C. | C | D. | D |
18.下列离子方程式书写正确的是( )
| A. | 向50 mL 1 mol•L-1明矾溶液中滴入少量0.1 mol•L-1Ba(OH)2溶液Al3++2SO42-+2Ba2++3OH-═Al(OH)3↓+2BaSO4↓ | |
| B. | 已知还原性Fe2+>Br-,a mol FeBr2溶液中通入a mol Cl2:2Fe2++2Br-+2Cl2═Br2+2Fe3++4C1- | |
| C. | 向KI与稀硫酸的混合溶液中通入氧气:4H++O2+6I-═3I2+2H2O | |
| D. | 在澄清石灰水中加入适量碳酸氢镁溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
5.化学与人类关系密切.下列有关物质的用途及其解释的说法正确的是( )
| 物质用途 | 解释 | |
| A | 食醋浸泡水壶中的水垢 | 水垢中CaCO3溶于醋酸,酸性H2CO3>CH3COOH |
| B | 炒菜时加一点酒和醋 | 有酯类物质生成,使菜味香可口 |
| C | NaClO溶液可用作洗手液 | NaClO具有杀菌、消毒作用 |
| D | Al2O3可用作医药中的胃酸中和剂 | Al2O3能与胃酸反应,使胃液酸度降低 |
| A. | A | B. | B | C. | C | D. | D |
3.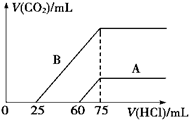 (1)取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
(1)取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
①原NaOH溶液的物质的量浓度为0.75mol/L.
②曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是Na2CO3、NaOH,其物质的量之比为1:3.
③曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为112mL.
(2)现有甲、乙两瓶无色溶液,已知它们可能为AlCl3溶液和NaOH溶液.现分别将一定体积的甲、乙两溶液混合,具体情况如下表所示,请回答:
①甲瓶溶液为AlCl3溶液.
②乙瓶溶液的物质的量浓度为0.5mol/L.
 (1)取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
(1)取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:①原NaOH溶液的物质的量浓度为0.75mol/L.
②曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是Na2CO3、NaOH,其物质的量之比为1:3.
③曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为112mL.
(2)现有甲、乙两瓶无色溶液,已知它们可能为AlCl3溶液和NaOH溶液.现分别将一定体积的甲、乙两溶液混合,具体情况如下表所示,请回答:
| 实验① | 实验② | 实验③ | |
| 取甲瓶溶液的量 | 400mL | 120mL | 120mL |
| 取乙瓶溶液的量 | 120mL | 440mL | 400mL |
| 生成沉淀的量 | 1.56g | 1.56g | 3.12g |
②乙瓶溶液的物质的量浓度为0.5mol/L.

 ;
;