题目内容
 已知氧化性强弱顺序为BrO3->ClO3->Cl2>IO3->Br2>I2.某同学为验证其中某些离子的氧化性进行如下实验.向盛有30mL 0.2mol?L-1 KI溶液的锥形瓶中滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液至过量.
已知氧化性强弱顺序为BrO3->ClO3->Cl2>IO3->Br2>I2.某同学为验证其中某些离子的氧化性进行如下实验.向盛有30mL 0.2mol?L-1 KI溶液的锥形瓶中滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液至过量.(1)开始滴加KBrO3溶液时的现象为
(2)KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是
(3)滴加KBrO3溶液至过量时观察到溶液褪色,其可能的原因是(用化学方程式表示)
(4)若用y表示锥形瓶中含碘物质的物质的量,用x表示所滴入KBrO3的物质的量,在下图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标).
考点:氯、溴、碘及其化合物的综合应用,氧化性、还原性强弱的比较
专题:卤族元素
分析:(1)根据n=cV计算溶液中n(I-),反应中I-是还原剂,被氧化为I2,碘单质遇到淀粉变蓝,化合价由-1价升高为0价,据此计算;
(2)KBrO3溶液与KBr溶液在酸性条件下,发生类似信息反应③的反应,BrO3-、Br-在酸性条件下生成溴单质与水;
(3)滴加KBrO3溶液至过量时观察到溶液的蓝色逐渐褪去,说明I2被氧化,该反应只能说明I2的还原性比Br2强,;
(4)先发生①BrO3-+6I-+6H+=3I2+Br-+3H2O,0.006molI-完全反应生成0.003molI2、0.001molBr-,消耗0.001molBrO3-,再发生反应BrO3-+5Br-+6H+=3Br2+3H2O,0.001molBr-完全反应消耗0.0002molBrO3-,最后发生反应②2BrO3-+I2=2IO3-+Br2,0.003molI2完全反应生成0.006molIO3-,消耗0.006molBrO3-,据此作图.
(2)KBrO3溶液与KBr溶液在酸性条件下,发生类似信息反应③的反应,BrO3-、Br-在酸性条件下生成溴单质与水;
(3)滴加KBrO3溶液至过量时观察到溶液的蓝色逐渐褪去,说明I2被氧化,该反应只能说明I2的还原性比Br2强,;
(4)先发生①BrO3-+6I-+6H+=3I2+Br-+3H2O,0.006molI-完全反应生成0.003molI2、0.001molBr-,消耗0.001molBrO3-,再发生反应BrO3-+5Br-+6H+=3Br2+3H2O,0.001molBr-完全反应消耗0.0002molBrO3-,最后发生反应②2BrO3-+I2=2IO3-+Br2,0.003molI2完全反应生成0.006molIO3-,消耗0.006molBrO3-,据此作图.
解答:
解:(1)溶液中n(I-)=0.03L×0.2mol?L-1=0.006mol,反应中I-是还原剂,被氧化为I2,碘单质遇到淀粉变蓝,化合价由-1价升高为0价,故转移电子物质的量为0.006mol×1=0.006mol;
故答案为:溶液由无色变为蓝色,0.006;
(2)BrO3-、Br-在酸性条件下生成溴单质与水,反应离子方程式为:BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3-+5Br-+6H+=3Br2+3H2O;
(3)滴加KBrO3溶液至过量时观察到溶液的蓝色逐渐褪去,说明I2被氧化,发生反应2BrO3-+I2=2IO3-+Br2,该反应只能说明I2的还原性比Br2强,不能说明碘的非金属性强于溴,
故答案为:2BrO3-+I2=2IO3-+Br2;不能;该反应只能说明I2的还原性比Br2强;
(4)先发生①BrO3-+6I-+6H+=3I2+Br-+3H2O,0.006molI-完全反应生成0.003molI2、0.001molBr-,消耗0.001molBrO3-,
再发生反应BrO3-+5Br-+6H+=3Br2+3H2O,0.001molBr-完全反应消耗0.0002molBrO3-,
最后发生反应②2BrO3-+I2=2IO3-+Br2,0.003molI2完全反应生成0.006molIO3-,消耗0.006molBrO3-,
故整个过程中含碘物质的物质的量,随加入KBrO3的物质的量的关系图为:
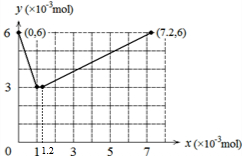
故答案为: .
.
故答案为:溶液由无色变为蓝色,0.006;
(2)BrO3-、Br-在酸性条件下生成溴单质与水,反应离子方程式为:BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3-+5Br-+6H+=3Br2+3H2O;
(3)滴加KBrO3溶液至过量时观察到溶液的蓝色逐渐褪去,说明I2被氧化,发生反应2BrO3-+I2=2IO3-+Br2,该反应只能说明I2的还原性比Br2强,不能说明碘的非金属性强于溴,
故答案为:2BrO3-+I2=2IO3-+Br2;不能;该反应只能说明I2的还原性比Br2强;
(4)先发生①BrO3-+6I-+6H+=3I2+Br-+3H2O,0.006molI-完全反应生成0.003molI2、0.001molBr-,消耗0.001molBrO3-,
再发生反应BrO3-+5Br-+6H+=3Br2+3H2O,0.001molBr-完全反应消耗0.0002molBrO3-,
最后发生反应②2BrO3-+I2=2IO3-+Br2,0.003molI2完全反应生成0.006molIO3-,消耗0.006molBrO3-,
故整个过程中含碘物质的物质的量,随加入KBrO3的物质的量的关系图为:

故答案为:
 .
.
点评:本题考查氧化还原反应及计算、对信息的利用,难度中等,是对学生综合能力的考查,注意滴加过程中BrO3-氧化Br-的反应.

练习册系列答案
相关题目
对于下列反应的反应类型判断,不正确的是( )
| A、CO2+H2O═H2CO3 化合反应 | ||||
B、Cu(OH)2
| ||||
C、Fe2O3+3CO
| ||||
| D、NaCl+AgNO3═AgCl↓NaNO3 复分解反应 |
某溶液中只含有Mg2+、Al3+、Cl-、S
四种离子,已知前三种离子的个数比为3:2:4,则溶液中Mg2+和S
的离子个数比为( )
| O | 2- 4 |
| O | 2- 4 |
| A、3:2 | B、3:4 |
| C、1:2 | D、1:4 |
将下列物质按酸、碱、盐分类顺序排列,正确的是( )
| A、硫酸、烧碱、纯碱 |
| B、硫酸、纯碱、食盐 |
| C、碳酸、乙醇、高锰酸钾 |
| D、磷酸、熟石灰、生石灰 |
 如右图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如右图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A、反应③最多能产生0.05mol O2 |
| B、反应①的离子方程式为:Na+2H2O═Na++2OH-+H2↑ |
| C、Na2O2中阴阳离子数目之比为1:1 |
| D、①、②、③充分反应后所得溶液的质量分数从大到小:①>②>③ |
 化学是一门以实验为主的科学,化学实验是学习探究物质性质的基本方法之一.
化学是一门以实验为主的科学,化学实验是学习探究物质性质的基本方法之一.