题目内容
16.下列说法中,正确的是( )| A. | 化合物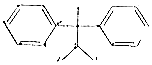 是苯的同系物 是苯的同系物 | |
| B. | 有机物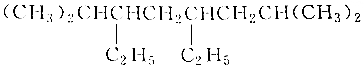 的系统名称是2-甲基-4-乙基-6-异丙基辛烷 的系统名称是2-甲基-4-乙基-6-异丙基辛烷 | |
| C. | C4H8的同分异构体只有3种 | |
| D. | 液化石油气的主要成分是烃,它是一种清洁燃料 |
分析 A.苯的同系物中必须只含有1个苯环;
B.主链选取除去,不满足侧链最简原则;
C.C4H8可能为烯烃或环烷烃,其同分异构体不止3种;
D.液化石油气的主要成分是乙烯、乙烷、丙烷、丙烯、丁烷、丁烯等.
解答 解:A.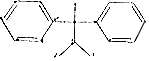 中含有2个苯环,与苯的结构不相似,则该有机物不属于苯的同系物,故A错误;
中含有2个苯环,与苯的结构不相似,则该有机物不属于苯的同系物,故A错误;
B.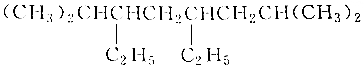 的主链为辛烷,编号从左边开始,在2、7号含有2个甲基,在3、5号碳含有2个乙基,该有机物正确名称为:2,7-二甲基-3,7-二乙基辛烷,故B错误;
的主链为辛烷,编号从左边开始,在2、7号含有2个甲基,在3、5号碳含有2个乙基,该有机物正确名称为:2,7-二甲基-3,7-二乙基辛烷,故B错误;
C.C4H8可能为烯烃,含有3种同分异构体,也可能为环丁烷或甲基丙烷,所以其同分异构体有5种,故C错误;
D.液化石油气的主要成分是烃,燃烧产物为二氧化碳和水,属于清洁燃料,故D正确;
故选D.
点评 本题考查同系物、同分异构体、有机物命名等知识,明确常见有机物命名原则为解答关键,注意掌握同分异构体的书写原则,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
6.醋酸溶液中存在电离平衡CH3COOH?H++CH3COO-,下列叙述正确的是( )
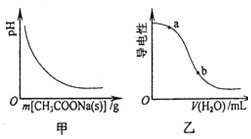

| A. | 图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化 | |
| B. | 图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b | |
| C. | 醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) | |
| D. | 0.10 mol•L-1的CH3COOH溶液中加水稀释,溶液中c(OH-)减小 |
7.在某温度下,将2molA和3molB充入一密闭容器中,发生反应:aA(g)+B(g)?C(g)+D(g),5min后达到平衡,测得K=1.若在温度不变的情况下将容器的体积扩大为原来的1倍,测得A的转化率不发生变化,下列说法正确的是( )
| A. | 改变条件前后,B的转化率均为40% | |
| B. | 改变条件前后,C的反应速率保持不变 | |
| C. | 若保持温度和体积不变,在容器中再充入1molA和1molB,B的转化率不变 | |
| D. | 若保持温度和体积不变,在容器中再充入0.5molB、1molC和1molD,B的转化率增大 |
4.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是( )
| A. | NaOH | B. | KMnO4 | C. | KSCN | D. | 氯水 |
11.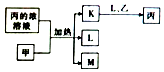 短周期主族元素W、X、Y、Z的原子序数依次增加,K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体.K是无色气体,是主要的大气污染物之一,0.05mol/L丙溶液的pH为l,上述物质的转化关系如图所示.下列说法正确的是( )
短周期主族元素W、X、Y、Z的原子序数依次增加,K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体.K是无色气体,是主要的大气污染物之一,0.05mol/L丙溶液的pH为l,上述物质的转化关系如图所示.下列说法正确的是( )
 短周期主族元素W、X、Y、Z的原子序数依次增加,K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体.K是无色气体,是主要的大气污染物之一,0.05mol/L丙溶液的pH为l,上述物质的转化关系如图所示.下列说法正确的是( )
短周期主族元素W、X、Y、Z的原子序数依次增加,K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体.K是无色气体,是主要的大气污染物之一,0.05mol/L丙溶液的pH为l,上述物质的转化关系如图所示.下列说法正确的是( )| A. | 原子半径:W<X<Y | B. | 元素的非全属性:Z>Y>X | ||
| C. | 化合物XYZ中只含共价键 | D. | K、L、M中沸点最高的是M |
10.常温下,根据表中的几种物质的电离平衡常数回答下列问题:
(1)常温下,等浓度的NH4NO3和NH4NO2两份溶液,测得NH4NO2溶液中c(NH4+)较小,试分析原因:NO2-水解显碱性,对铵根离子水解起到促进作用.0.1mol•L-1NH4NO2溶液中离子浓度由大到小的顺序是c(NO2-)>c(NH4+)>c(H+)>c(OH-),NO2-水解反应的平衡常数Kh=1.4×10-11 mol•L-1(保留两位有效数字).
(2)常温下,用氨水吸收CO2得到NH4HCO3溶液,其pH>7 (填“>”、“<”或“=”);反应NH3•H2O+H2CO3?NH4++HCO3-+H2O的平衡常数K=800.
(3)少量CO2通入到过量的NaClO溶液中发生反应的离子方程式ClO-+CO2+H2O═HCO3-+HClO:
| NH3•H2O | 2×10-5 |
| HNO2 | 7×10-4 |
| HClO | 3×10-8 |
| H2CO3 | K1=4×10-7 K2=4×10-11 |
(2)常温下,用氨水吸收CO2得到NH4HCO3溶液,其pH>7 (填“>”、“<”或“=”);反应NH3•H2O+H2CO3?NH4++HCO3-+H2O的平衡常数K=800.
(3)少量CO2通入到过量的NaClO溶液中发生反应的离子方程式ClO-+CO2+H2O═HCO3-+HClO:
7.地下水受到硝酸盐污染已成为世界范围内一个相当普遍的环境问题.用零价铁去除水体中的硝酸盐(NO3-)是地下水修复研究的热点之一.
(1)Fe还原水体中NO3-的反应原理如图1所示.
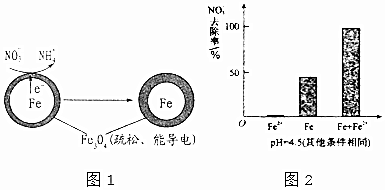
作负极的物质是铁;正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)将足量铁粉投入水体中,测定NO3-去除率和pH,结果如表:
在pH=4.5的水体中,NO3-的去除率低的原因是FeO(OH)不导电,阻碍电子转移.
(3)为提高pH=4.5的水体中NO3-的去除率,某课题组在初始pH=4.5的水体中分别投入①Fe2+、②Fe、③Fe和Fe2+做对比实验结果如图2:①此实验可得出的结论是本实验条件下,Fe2+不能直接还原NO3-,在Fe和Fe2+共同作用下能提高NO3-的去除率,Fe2+的作用可能是Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4.表中NO3-去除率和铁的最终物质形态不同的原因初始pH低时,产生的Fe2+充足;初始pH高时,产生的Fe2+不足.
(4)地下水呈中性,在此条件下,要提高NO3-的去除速率,可采取的措施有减小铁粉的颗粒大小,增大反应接触面积或加入活性炭,形成微电池.(写出一条)
(1)Fe还原水体中NO3-的反应原理如图1所示.

作负极的物质是铁;正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)将足量铁粉投入水体中,测定NO3-去除率和pH,结果如表:
| 初始pH | pH=2.5 | pH=4.5 |
| 1小时pH | 接近中性 | 接近中性 |
| 24小时pHNO3-的去除率 | 接近100% | <50% |
| 铁的最终物质形态 | 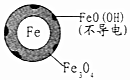 | 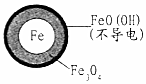 |
(3)为提高pH=4.5的水体中NO3-的去除率,某课题组在初始pH=4.5的水体中分别投入①Fe2+、②Fe、③Fe和Fe2+做对比实验结果如图2:①此实验可得出的结论是本实验条件下,Fe2+不能直接还原NO3-,在Fe和Fe2+共同作用下能提高NO3-的去除率,Fe2+的作用可能是Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4.表中NO3-去除率和铁的最终物质形态不同的原因初始pH低时,产生的Fe2+充足;初始pH高时,产生的Fe2+不足.
(4)地下水呈中性,在此条件下,要提高NO3-的去除速率,可采取的措施有减小铁粉的颗粒大小,增大反应接触面积或加入活性炭,形成微电池.(写出一条)
8.设NA为阿伏加德罗常教,下列叔述正确的是( )
| A. | 常温常压下,9.2gNO2气体中.分子数为0.2NA | |
| B. | pH=2的硫酸溶液中,H+数目为0.01NA | |
| C. | 将0.05molFeCl3全部转化为Fe(OH)3胶体,则胶粒数目为0.05NA | |
| D. | 20gD2O中含有的质子数为10NA |

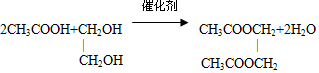 .
.