题目内容
15.图1是某课外小组设计在实验室制取氨气的装置图,请依据要求,回答下列问题.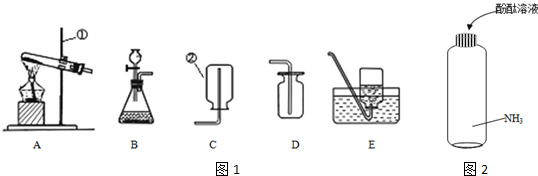
(1)写出带标号的仪器的名称:①铁架台;②集气瓶.
(2)实验室利用浓氨水和生石灰制取氨气应选择的装置为(填代号)B,用氯化铵与氢氧化钙制取氨气时,应选择的装置为(填代号)A.收集氨气应装置为(填代号)C. 若要得到干燥的氨气,需用作碱石灰(填“浓硫酸”或“碱石灰”或“P2O5”)干燥剂.
(3)在如图2所示的一无色透明塑料矿泉水瓶中充满氨气,现将少量酚酞溶液注入瓶中,迅速盖紧瓶盖,并进行振荡,则观察到的现象是溶液变红色
(4)写出实验室用氯化铵与氢氧化钙制取氨气的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2.
分析 (1)图形分析可知①为铁架台,②为集气瓶;
(2)实验室利用浓氨水和生石灰制取氨气,把浓氨水滴入生石灰溶解反应放出的热量使一水合氨分解,氨气挥发出,用氯化铵与氢氧化钙制取氨气时需要加热反应,结合固体和固体加热制备气体原理选择发生装置,氨气极易溶于水,比空气轻,收集方法为向下排空气法收集,氨气是碱性气体,干燥需要通过固体干燥剂碱石灰;
(3)氨气溶于水生成一水合氨,溶液中一水合氨电离出氢氧根离子溶液显碱性;
(4)实验室用氯化铵与氢氧化钙制取氨气,加热生成氨气、水、氯化钙.
解答 解:(1)图形分析可知带标号的仪器的名称:①为铁架台,②为集气瓶,
故答案为:铁架台;集气瓶;
(2)实验室利用浓氨水和生石灰制取氨气不需要加热,只需要把浓氨水滴入生石灰,氧化钙溶解反应生成氢氧化钙过程中放出的热量,一水合氨分解,氨气挥发出,反应不需要加热,选择装置B进行,用氯化铵与氢氧化钙制取氨气时需要加热反应,结合固体和固体加热制备气体原理选择发生装置A,氨气极易溶于水,比空气轻,收集方法为向下排空气法收集,收集氨气选择C,氨气是碱性气体,干燥需要通过固体干燥剂碱石灰,
故答案为:B;A;C;碱石灰;
(3)氨气溶于水生成一水合氨,溶液中一水合氨电离出氢氧根离子溶液显碱性,NH3•H2O?NH4++OH-,溶液显碱性遇到酚酞试液变红色,
故答案为:溶液变红色;
(4)实验室用氯化铵与氢氧化钙制取氨气,加热生成氨气、水、氯化钙,反应的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2.
点评 本题考查了实验室制备氨气的发生装置选择、原理分析、收集气体的方法、氨气性质等知识点,掌握基础是解题关键,题目难度中等.

| 测定时间/min | 0 | 1 | 2 | 4 | 5 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
②我国是燃煤大国,若某家庭取暖每天燃烧 6.4kg 煤,煤中硫元素的质量分数为 1%.假设煤中的硫全部转化为 SO2,试计算每天产生的 SO2的体积(标准状况下).
③治理燃煤大都采用的是石灰石-石膏法脱硫,试写出脱硫过程中发生反应的主要化学方程式,CaCO3+SO2$\frac{\underline{\;高温\;}}{\;}$CaSO3+CO2,2CaSO3+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4.
| A. | 原子半径C>D>A>B | B. | 离子半径D>C>B>A | ||
| C. | 原子序数b>a>c>d | D. | 单质的还原性A>B>C>D |
| A. | 0.1mol﹒L-1CH3COOH溶液中:c(CH3COO-)+c(OH-)=c(H+) | |
| B. | 0.1mol﹒L-1CuSO4溶液中:c(SO42-)>c(Cu2+)>c(OH-)>c(H+) | |
| C. | 室温下,pH=2的HCl溶液与pH=12的氨水等体积混合后的溶液中:c(Cl-)>c(NH4+) | |
| D. | 物质的量浓度相同的HCl溶液与氨水等体积混合后的溶液中:c(Cl-)=c(NH4+) |
| A. | Na2O | B. | CO2 | C. | KCl | D. | NaOH |
| A. | 81 | B. | 80 | C. | 79 | D. | 78 |
| A. | CH4 | B. | C6H6 | C. | CH3-CH3 | D. | CH3Cl |