题目内容
19.一定量的铝溶于一定浓度的硝酸的反应中,产生标准状况下的NO气体11.2L,在所得溶液中加入足量的氨水,完全反应后过滤出沉淀,经洗涤、蒸干并充分灼烧,最后得到固体的质量为( )| A. | 25.5g | B. | 39g | C. | 51g | D. | 106.5g |
分析 由题意可知,加入氢氧化钠后所得沉淀为氢氧化铝,蒸干并充分灼烧,最后得到固体为氧化铝,在金属与硝酸的反应中,金属提供的电子的物质的量等于硝酸中氮元素的得电子的物质的量,硝酸被还原为NO,根据n=$\frac{V}{{V}_{m}}$计算NO的物质的量,根据氮元素的化合价变化计算转移电子物质的量,利用电子转移守恒计算n(Al)根据镁原子守恒可知n(Al2O3)=$\frac{1}{2}$n(Al),再根据m=nM计算氧化铝的质量.
解答 解:标准状况下11.2LNO气体的物质的量为:$\frac{11.2L}{22.4L/mol}$=0.5mol,
金属提供的电子的物质的量等于硝酸中氮元素的得电子的物质的量,故3×n(Al)=n(NO)×(5-2),即:n(Al)=n(NO)=0.5mol,
则最后得到的氧化铝的物质的量为:n(Al2O3)=$\frac{1}{2}$n(Al)=0.25mol,
所以最后得到固体的质量为:m(Al2O3)=0.25mol×102g/mol=25.5g,
故选A.
点评 本考查氧化还原反应有关计算,题目难度中等,根据电子转移守恒计算氧化镁的物质的量是解题关键,注意氧化还原反应中守恒思想的运用,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
9.将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,则( )
| A. | 反应过程中得到8.96 L的气体 | B. | 最终得到的溶液中溶质为NaCl | ||
| C. | 最终Al元素全部以沉淀形式存在 | D. | 最终得到的溶液中n(NaCl)=0.3 mol |
7.现有常温时pH=1的某强酸溶液10mL,下列操作能使溶液的pH变成2的是( )
| A. | 加水稀释成100 mL | B. | 加入10 mL的水进行稀释 | ||
| C. | 加入10 mL 0.01 mol/L的NaOH溶液 | D. | 加入10 mL 0.01 mol/L的HCl溶液 |
8.下列大小关系正确的是( )
| A. | 熔点:HI<HBr | B. | 硬度:MgO>CaO | ||
| C. | 晶格能:NaCl<NaBr | D. | 熔沸点:CO2>NaCl |
2.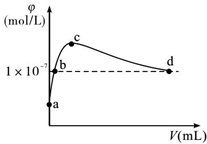 常温下,将CO2通入2LpH=12的KOH溶液中.溶液中水电离出的OH-离子浓度(φ)与通入的CO2的体积(V)的关系如图所示.下列叙述不正确的是( )
常温下,将CO2通入2LpH=12的KOH溶液中.溶液中水电离出的OH-离子浓度(φ)与通入的CO2的体积(V)的关系如图所示.下列叙述不正确的是( )
 常温下,将CO2通入2LpH=12的KOH溶液中.溶液中水电离出的OH-离子浓度(φ)与通入的CO2的体积(V)的关系如图所示.下列叙述不正确的是( )
常温下,将CO2通入2LpH=12的KOH溶液中.溶液中水电离出的OH-离子浓度(φ)与通入的CO2的体积(V)的关系如图所示.下列叙述不正确的是( )| A. | a点溶液中:水电离出的c(H+)=1×10-12mol/L | |
| B. | b点溶液中:c(H+)=1×10-7mol/L | |
| C. | c点溶液中:c(K+)=2[c(CO${\;}_{3}^{2-}$)+c(HCO3-)+c(H2CO3)] | |
| D. | d点溶液中:c(K+)=2c(CO${\;}_{3}^{2-}$)+c(HCO${\;}_{3}^{-}$) |