题目内容
下表是元素周期表的一部分,根据A-K在周期表中的位置,用元素符号或化学式回答下列问题.
(1)写出D、G的元素符号 、
(2)A到K中化学性质最不活泼的是
(3)最高价氧化物对应的水化物碱性最强的是 (写化学式、下同),酸性最强的是
(4)C的氢氧化物与I的氢化物反应的化学方程式:
(5)请设计一个实验比较I和K单质氧化性的强弱 写出该反应的离子方程式为 .
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | F | H | |||||
| 3 | B | C | E | G | I | J | ||
| 4 | K |
(2)A到K中化学性质最不活泼的是
(3)最高价氧化物对应的水化物碱性最强的是
(4)C的氢氧化物与I的氢化物反应的化学方程式:
(5)请设计一个实验比较I和K单质氧化性的强弱
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:(1)由元素在周期表中位置,可知A为氢,B为Na,C为Al,D为碳,E为Si,F为氮,G为磷,H为氟,I为Cl,J为Ar,K为Br;
(2)稀有气体的化学性质最不活泼;
(3)上述元素中Na的金属性最强,故氢氧化钠碱性最强,F元素没有最高价含氧酸,上述元素中,最高价含氧酸中高氯酸的酸性最强;
(4)氢氧化铝与盐酸反应生成氯化铝与水;
(5)利用单质之间的相互置换进行验证.
(2)稀有气体的化学性质最不活泼;
(3)上述元素中Na的金属性最强,故氢氧化钠碱性最强,F元素没有最高价含氧酸,上述元素中,最高价含氧酸中高氯酸的酸性最强;
(4)氢氧化铝与盐酸反应生成氯化铝与水;
(5)利用单质之间的相互置换进行验证.
解答:
解:(1)由元素在周期表中位置,可知A为氢,B为Na,C为Al,D为碳,E为Si,F为氮,G为磷,H为氟,I为Cl,J为Ar,K为Br,故答案为:C;P;
(2)稀有气体Ar的化学性质最不活泼,故答案为:Ar;
(3)上述元素中Na的金属性最强,故NaOH的碱性最强,F元素没有最高价含氧酸,上述元素中,最高价含氧酸中HClO4的酸性最强,故答案为:NaOH;HClO4;
(4)氢氧化铝与盐酸反应生成氯化铝与水,反应方程式为:Al(OH)3+3HCl=AlCl3+3H2O,
故答案为:Al(OH)3+3HCl=AlCl3+3H2O;
(5)利用单质之间的相互置换进行验证,具体方案为:将氯水滴入溴化钠溶液中颜色变深,有关离子方程式为:Cl2+2Br-=2Cl-+Br2,
故答案为:将氯水滴入溴化钠溶液中颜色变深;Cl2+2Br-=2Cl-+Br2.
(2)稀有气体Ar的化学性质最不活泼,故答案为:Ar;
(3)上述元素中Na的金属性最强,故NaOH的碱性最强,F元素没有最高价含氧酸,上述元素中,最高价含氧酸中HClO4的酸性最强,故答案为:NaOH;HClO4;
(4)氢氧化铝与盐酸反应生成氯化铝与水,反应方程式为:Al(OH)3+3HCl=AlCl3+3H2O,
故答案为:Al(OH)3+3HCl=AlCl3+3H2O;
(5)利用单质之间的相互置换进行验证,具体方案为:将氯水滴入溴化钠溶液中颜色变深,有关离子方程式为:Cl2+2Br-=2Cl-+Br2,
故答案为:将氯水滴入溴化钠溶液中颜色变深;Cl2+2Br-=2Cl-+Br2.
点评:本题考查元素周期表与元素周期律综合应用,难度不大,注意掌握非金属性、金属性强弱比较及实验事实.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
设NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )
| A、常温常压下,48gO3含有的氧原子数为3NA |
| B、1.8g的NH4+离子中含有的电子数为NA |
| C、物质的量浓度为0.5mol/L Mg Cl2溶液,含有Cl-离子数为NA |
| D、标准状况下,11.2 L氧气所含的原子数为NA |
下列关于化工生产原理的叙述中,均符合目前工业生产实际的是( )
| A、氯碱工业中,电解槽的阳极区产生NaOH |
| B、氯气和氢气混合在光照条件下反应生成氯化氢,用水吸收得到盐酸 |
| C、合成氨工业中,由于氨易液化,N2、H2循环使用,所以总体上氨的产率很高 |
| D、二氧化硫在接触室被氧化成三氧化硫,三氧化硫在吸收塔内被水吸收制成浓硫酸 |
只用一种试剂,区别甲苯,四氯化碳,己烯,乙醇,碘化钾溶液,亚硫酸6种无色溶液,应选用( )
| A、酸性KMnO4溶液 |
| B、溴水 |
| C、碘水 |
| D、硝酸银溶液 |
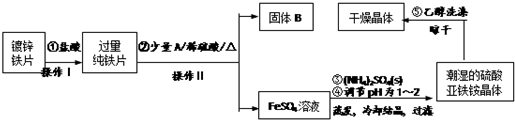
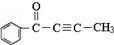 的有机物分子中:在同一直线上的碳原子最多有
的有机物分子中:在同一直线上的碳原子最多有 在20℃时,在一刚性容器内部有一个不漏气且可滑动的活塞将容器分隔成左右两室.左室充入氮气,右室充入氢气与氧气的混和气体,活塞恰好停留在离左端的
在20℃时,在一刚性容器内部有一个不漏气且可滑动的活塞将容器分隔成左右两室.左室充入氮气,右室充入氢气与氧气的混和气体,活塞恰好停留在离左端的