题目内容
11.下列解释对应事实的方程式中合理的是( )| A. | 用食醋清洗茶壶上的水垢:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | Fe(SCN)3溶液中滴NaOH溶液:Fe(SCN)3+3OH-═Fe(OH)3↓+3SCN- | |
| C. | 碳酸钠溶液显碱性:CO32-+2H2O?H2CO3+2OH- | |
| D. | 钠在空气中加热燃烧:4Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$2Na2O |
分析 A.醋酸为弱酸,离子方程式中醋酸不能拆开;
B.硫氰化铁为络合物,离子方程式中需要保留化学式;
C.碳酸根离子的水解分步进行,水解的离子方程式需要分步写,主要以第一步为主;
D.钠在空气中不加热、不点燃条件下氧化生成氧化钠,钠燃烧生成的是过氧化钠.
解答 解:A.醋酸和碳酸钙都需要保留化学式,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故A错误;
B.Fe(SCN)3溶液中滴NaOH溶液,反应生成氢氧化铁沉淀和硫氢化钠,反应的离子方程式为:Fe(SCN)3+3OH-═Fe(OH)3↓+3SCN-,故B正确;
C.碳酸钠溶液显碱性,碳酸根离子的水解方程式需要分步书写,主要写出第一步即可,正确的离子方程式为:CO32-+H2O?HCO3-+OH-,故C错误;
D.钠在空气中燃烧生成过氧化钠,正确的化学方程式为:2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2,故D错误;
故选B.
点评 本题考查了离子方程式、化学方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式、化学方程式的书写原则,明确正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
1.下列离子方程式中正确的是( )
| A. | 氢氧化钠溶液吸收过量的二氧化碳:OH-+CO2═HCO3- | |
| B. | 亚硫酸氢铵溶液与足量氢氧化钠溶液反应:HSO3-+OH-═SO32-+H2O | |
| C. | 氯气通入冷水中:Cl2+H2O═Cl-+ClO-+2H+ | |
| D. | 碳酸镁悬浊液中加醋酸:CO32-+2CH3COOH═2CH3COO-+CO2↑+H2O |
16.把X溶液逐滴滴入Y溶液中,与把Y溶液逐滴滴入X溶液中,所产生的现象相同的是( )
| A | B | C | D | |
| X | HCl | BaCl2 | Na2CO3 | Al2(SO4)3 |
| Y | NaAlO2 | H2SO4 | H2SO4 | NaAlO2 |
| A. | A | B. | B | C. | C | D. | D |
2.逻辑推理是化学学习中常用的思维方法.下列推理结果正确的是( )
| A. | 酸碱中和反应生成盐和水,则生成盐和水的反应一定是中和反应 | |
| B. | 氧化物中都含有氧元素,则含有氧元素的化合物一定是氧化物 | |
| C. | 碱溶液的pH>7,则pH>7的溶液一定是碱的溶液 | |
| D. | 点燃H2和O2的混合气体可能发生爆炸,则H2点燃前须检验纯度 |
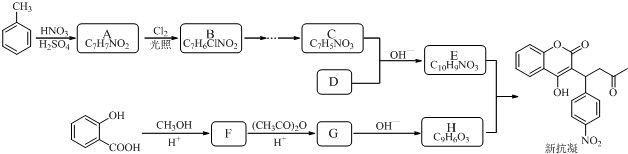
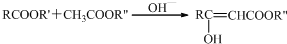
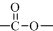 结构;
结构;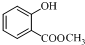 +(CH3CO)2O$\stackrel{H+}{→}$
+(CH3CO)2O$\stackrel{H+}{→}$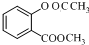 +CH3COOH.
+CH3COOH.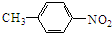 .
.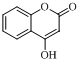 +CH3OH.
+CH3OH. .
.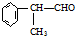 的物质,该物质是一种香料.
的物质,该物质是一种香料.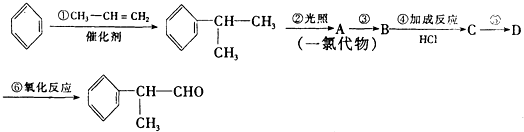
 .
. +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2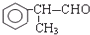 +2H2O.
+2H2O.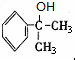 生成
生成 、
、 、
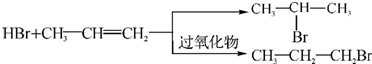
、 .
.
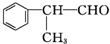 的物质,该物质是一种香料.
的物质,该物质是一种香料.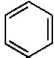 $→_{CH_{3}-CH=CH_{2}}^{①催化剂}$
$→_{CH_{3}-CH=CH_{2}}^{①催化剂}$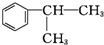 $→_{Br_{2}}^{②光照}$A(一溴代物)$\stackrel{③}{→}$B$→_{HBr}^{④加成反应}$C$\stackrel{⑤}{→}$ D$\stackrel{⑥氧化反应}{→}$
$→_{Br_{2}}^{②光照}$A(一溴代物)$\stackrel{③}{→}$B$→_{HBr}^{④加成反应}$C$\stackrel{⑤}{→}$ D$\stackrel{⑥氧化反应}{→}$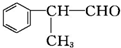
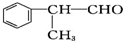 含有的官能团的名称为醛基.
含有的官能团的名称为醛基.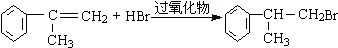 (有机物写结构简式,并注明反应条件,下同).
(有机物写结构简式,并注明反应条件,下同).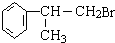 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$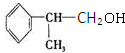 +NaBr.
+NaBr. 的水解产物
的水解产物 不能经氧化反应⑥而得到产品,导致产率低.
不能经氧化反应⑥而得到产品,导致产率低. 或
或 .
.