题目内容
14.下列关于元素周期律的叙述正确的是( )| A. | 随着元素原子序数的递增,原子最外层电子总是从1到8重复出现 | |
| B. | 随着元素原子序数的递增,原子半径从大到小(稀有气体除外)发生周期性变化 | |
| C. | 随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 | |
| D. | 元素性质的周期性变化是指原子核外电子排布的周期性变化、原子半径的周期性变化 |
分析 A.第一周期只有2种元素;
B.同周期,从左向右原子半径减小;同主族,从上到下原子半径增大;
C.第二周期中O、F没有正价;
D.原子核外电子排布的周期性变化引起元素性质的周期性变化.
解答 解:A.第一周期只有2种元素,则原子最外层电子从1到2,故A错误;
B.同周期从左向右原子半径减小,同主族从上到下原子半径增大,则随着元素原子序数的递增,原子半径从大到小(稀有气体除外)发生周期性变化,故B正确;
C.第二周期中O、F没有正价,从第三周期开始随着元素原子序数的递增,元素最高正价从+1到+7,且金属无负价,故C错误;
D.原子核外电子排布的周期性变化引起元素性质的周期性变化,元素性质的周期性变化指的是金属性、非金属性、元素的化合价、原子半径等,故D错误;
故选B.
点评 本题考查元素周期表和周期律的综合应用,为高频考点,把握元素的位置、元素的性质为解答的关键,侧重分析与应用能力的考查,注意周期律的实质,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.
【实验原理】2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢.该小组设计了如下的方案.
(1)已知反应后H2C2O4转化为CO2逸出,KMnO4转化为MnSO4,每消耗1mol H2C2O4转移2mol 电子,为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为:n(H2C2O4):n(KMnO4)≥2.5.
(2)探究温度对化学反应速率影响的实验编号是②和③(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是①和②.
(3)实验①测得KMnO4溶液的褪色时间t1为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=0.010或1.0×10-2 mol•L-1•min-1.
(4)已知50℃时c(MnO4-)~反应时间t的变化曲线如图1.若保持其他条件不变,请在答题卡坐标图中,画出25℃时c(MnO4-)~t的变化曲线示意图.
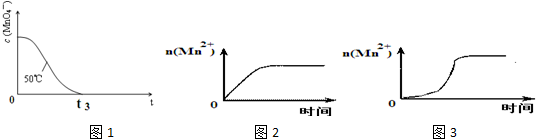
(5)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图2所示.但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图3所示.该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究.
①该小组同学提出的假设是生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用).
②请你帮助该小组同学完成实验方案,并填写表中空白.
③若该小组同学提出的假设成立,应观察到的现象是与实验1比较,溶液褪色所需时间短或所用时间(t)小于40s.
【实验原理】2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢.该小组设计了如下的方案.
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | 溶液颜色褪至无色所需时间/s | ||
| 浓度 /mol•L-1 | 体积 /mL | 浓度 /mol•L-1 | 体积 /mL | |||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 | t1 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 | t2 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 | t3 |
(2)探究温度对化学反应速率影响的实验编号是②和③(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是①和②.
(3)实验①测得KMnO4溶液的褪色时间t1为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=0.010或1.0×10-2 mol•L-1•min-1.
(4)已知50℃时c(MnO4-)~反应时间t的变化曲线如图1.若保持其他条件不变,请在答题卡坐标图中,画出25℃时c(MnO4-)~t的变化曲线示意图.

(5)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图2所示.但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图3所示.该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究.
①该小组同学提出的假设是生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用).
②请你帮助该小组同学完成实验方案,并填写表中空白.
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度 /℃ | 再向试管中加入少量固体 | 溶液颜色褪至无色所需时间/s | ||
| 浓度 /mol•L-1 | 体积 /mL | 浓度 /mol•L-1 | 体积 /mL | ||||
| ④ | 0.10 | 2.0 | 0.010 | 4.0 | 25 | MnSO4 | t4 |
2.Fe3+和I-在水溶液中的反应如下:2I-+2Fe3+?2Fe2++I2(水溶液)
(1)在一定温度下,测得2min内生成I2的物质的量浓度为0.02mol/L,则用Fe3+表示该反应在这2min内平均反应速率为0.02mol•L-1•min-1.
(2)假设c(I-)由0.1mol/L降到0.07mol/L需15s,那么c(I-)由0.07mol/L降到0.05mol/L,所需反应的时间为大于10s(填“大于”、“小于”或“等于”)
(3)上述反应的正反应速率和I-、Fe3+的物质的量浓度关系为:ν=k{c(I-)}m{c(Fe3+)}n(k为常数)
通过上表所给的数据计算,得知:ν=k{c(I-)}m{c(Fe3+)}n中,m、n的值为C(选填A、B、C、D)
A.m=1,n=1 B.m=1,n=2 C.m=2,n=1 D.m=2,n=2
(4)I-物质的量浓度对反应速率的影响大于(填“大于”、“小于”或“等于”)Fe3+物质的量浓度对反应速率的影响.
(1)在一定温度下,测得2min内生成I2的物质的量浓度为0.02mol/L,则用Fe3+表示该反应在这2min内平均反应速率为0.02mol•L-1•min-1.
(2)假设c(I-)由0.1mol/L降到0.07mol/L需15s,那么c(I-)由0.07mol/L降到0.05mol/L,所需反应的时间为大于10s(填“大于”、“小于”或“等于”)
(3)上述反应的正反应速率和I-、Fe3+的物质的量浓度关系为:ν=k{c(I-)}m{c(Fe3+)}n(k为常数)
| C(I-)/(mol•L-1) | C(Fe3+)/(mol•L-1) | ν/(mol•(L•s)-1) | |
| ① | 0.20 | 0.80 | 0.032k |
| ② | 0.60 | 0.40 | 0.144k |
| ③ | 0.80 | 0.20 | 0.128k |
A.m=1,n=1 B.m=1,n=2 C.m=2,n=1 D.m=2,n=2
(4)I-物质的量浓度对反应速率的影响大于(填“大于”、“小于”或“等于”)Fe3+物质的量浓度对反应速率的影响.
19.下列物质中,可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的是( )
| A. | 氢氧化钠溶液 | B. | 溴水 | C. | 碳酸钠溶液 | D. | 紫色石蕊溶液 |
6.将100mL 0.001mol•L-1的盐酸和50mL pH=3的硫酸溶液混合后,所得溶液的pH为( )
| A. | 4.5 | B. | 2.7 | C. | 3.3 | D. | 3 |
4.下列关于石油的成分与加工的说法错误的是( )
| A. | 天然气的化学组成主要是烃类气体,以甲烷为主 | |
| B. | 石油中含有1-50个碳原子的烷烃和环烷烃 | |
| C. | 石油的催化重整不可能获得芳香烃 | |
| D. | 石油的催化裂解是工业生产乙烯的重要环节 |
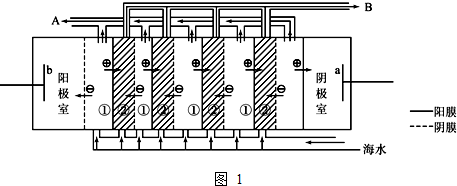

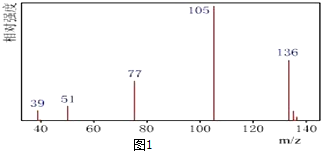
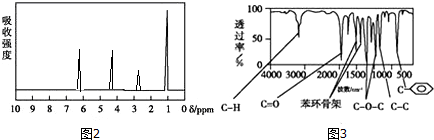
 .
.