题目内容
17.下列说法正确的是( )| A. | SiH4比CH4稳定 | |
| B. | P和As属于第ⅤA族元素,H3PO4酸性比H3AsO4的弱 | |
| C. | Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 | |
| D. | O2-半径比F-的小 |
分析 A.非金属性C>Si,非金属性越强,对应氢化物越稳定;
B.非金属性P>As,非金属性越强,对应最高价氧化物的水化物的酸性越强;
C.同主族从上到下金属性增强,金属性越强,失去电子能力越强;
D.具有相同电子排布的离子中,原子序数大的离子半径小.
解答 解:A.非金属性C>Si,则CH4比SiH4稳定,故A错误;
B.非金属性P>As,非金属性越强,对应最高价氧化物的水化物的酸性越强,则H3PO4酸性比H3AsO4的强,故B错误;
C.同主族从上到下金属性增强,金属性越强,失去电子能力越强,则Cs失电子能力比Na的强,故C正确;
D.具有相同电子排布的离子中,原子序数大的离子半径小,则O2-半径比F-的大,故D错误;
故选C.
点评 本题考查元素周期表和周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.下列各组离子在给定条件下一定能大量共存的是( )
| A. | 使pH试纸变蓝的溶液中:Fe3+、NH4+、S2-、SO32- | |
| B. | 能与Al反应产生H2的溶液中:HCO3-、Ba2+、Al3+、Br- | |
| C. | 常温下pH=1的溶液中:Mg2+、Cl-、SO42-、Fe3+ | |
| D. | 由水电离出的c(H+)=1×10-13 mol/L的溶液:K+、AlO2-、Br-、Cl- |
12.下列有关有机物的叙述不正确的是( )
| A. | C5H12O的醇有8种结构 | B. | 分子式为C4H8的链烃有2种 | ||
| C. | C4H8O2的酯有4种结构 | D. | C9H12含苯环的烃有8种 |
9.高氯酸是一种酸性极强的无机含氧酸,可用于制备高氯酸盐、人造金刚石提纯等方面.查阅资料得到以下有关高氯酸的信息:
工业上生产高氯酸的同时还生产了亚氯酸钠,工业流程如图:
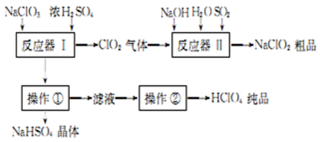
(1)操作①的名称是过滤,操作②的名称是蒸馏.
(2)反应器Ⅰ中发生反应的化学方程式为3NaClO3+3H2SO4=HClO4+2ClO2↑+3NaHSO4+H2O.
(3)反应器Ⅱ中发生反应的离子方程式为4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O.
(4)若反应器Ⅱ中SO2以H2O2代替也可达到同样的目,此时发生反应的离子方程式为2ClO2+2OH-+H2O2=2ClO2-+O2+2H2O.
(5)若想得到201 kg的 HClO4纯品,至少需要NaClO3 639 kg.
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸.写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)HCl+4H2O-8e-=HClO4+8H+.
| 名称 | 分子式 | 外观 | 沸点 |
| 高氯酸 | HClO4 | 无色液体 | 130℃ |

(1)操作①的名称是过滤,操作②的名称是蒸馏.
(2)反应器Ⅰ中发生反应的化学方程式为3NaClO3+3H2SO4=HClO4+2ClO2↑+3NaHSO4+H2O.
(3)反应器Ⅱ中发生反应的离子方程式为4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O.
(4)若反应器Ⅱ中SO2以H2O2代替也可达到同样的目,此时发生反应的离子方程式为2ClO2+2OH-+H2O2=2ClO2-+O2+2H2O.
(5)若想得到201 kg的 HClO4纯品,至少需要NaClO3 639 kg.
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸.写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)HCl+4H2O-8e-=HClO4+8H+.
5.在一密闭容器中充入1molH2和1molI2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g)=2HI(g)△H<0,下列条件能加快反应速率的是( )
| A. | 体积不变,向其中加入1mol H2 | |
| B. | 体积不变,向其中加入1mol N2 | |
| C. | 压强不变,向其中加入1mol N2 | |
| D. | 压强不变,向其中加入1mol H2和1molI2 |