题目内容
20.下列叙述不正确的是( )| A. | Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 | |
| B. | NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 | |
| C. | pH值相等的三种溶液:①NH4Cl ②(NH4)2SO4③NH4HSO4中c(NH4+)大小顺序为②>①>③ | |
| D. | 加热0.1 mol•L-1 Na2CO3溶液,CO32-的水解程度和溶液的pH均增大 |
分析 A、氯化铵水解显示酸性,可以促进氢氧化镁的溶解;
B、HF溶液不能存放于玻璃试剂瓶中,HF可以和二氧化硅之间反应;
C、①NH4Cl ②(NH4)2SO4③NH4HSO4中氨根离子的水解分别受到不同的影响;
D、加热0.1 mol•L-1 Na2CO3溶液可以促进碳酸根离子的水解,使得溶液碱性更强.
解答 解:A、氯化铵水解显示酸性,可以克氢氧根离子之间反应,促进氢氧化镁的溶解,故A正确;
B、NH4F水溶液水解 产生HF,HF可以和二氧化硅之间反应,溶液不能存放于玻璃试剂瓶中,故B正确;
C、①NH4Cl ②(NH4)2SO4③NH4HSO4中氨根离子的水解程度不同,分别是:无影响、无影响、抑制水解,但是②电离出的铵根离子浓度大于①③,所以c(NH4+)大小顺序为②>③>①,故C错误;
D、加热0.1 mol•L-1 Na2CO3溶液可以促进碳酸根离子的水解,使得溶液碱性更强,即CO32-的水解程度和溶液的pH均增大,故D正确.
故选C.
点评 本题综合考查学生沉淀溶解平衡、盐的水解原理等知识,属于综合知识的考查,难度中等.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
10.为了除去蛋白质溶液中混入的少量氯化钠,可以采用的方法是( )
| A. | 过滤 | B. | 盐析 | ||
| C. | 渗析 | D. | 加入AgNO3溶液,过滤 |
11.下列说法错误的是( )
| A. | 过渡元素全是d区元素 | B. | 非金属元素大多数在p区 | ||
| C. | 过渡元素全是金属元素 | D. | s区元素包括ⅠA族和ⅡA族元素 |
8.室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是( )
| A. | 溶液中导电粒子的数目减少 | |
| B. | 溶液中$\frac{{c(C{H_3}CO{O^-})}}{{c(C{H_3}COOH)•c(O{H^-})}}$不变 | |
| C. | 醋酸的电离程度增大,溶液酸性增强 | |
| D. | 再加入10mL pH=11的NaOH溶液,混合液pH=7 |
15.在溶液中能大量共存的离子组是( )
| A. | Fe3+、OH一、HCO3- | B. | Ba2+、OH一、C1- | C. | H+、K+、CO32-、 | D. | NH4+、NO3-、OH- |
5.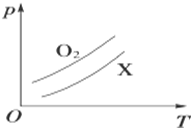 如图表示1g O2与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体不可能是( )
如图表示1g O2与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体不可能是( )
 如图表示1g O2与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体不可能是( )
如图表示1g O2与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体不可能是( )| A. | C2H6 | B. | CH4 | C. | CO2 | D. | SO2 |
11.下列热化学方程式或叙述正确的是( )
| A. | 1 mol液态肼在足量氧气中完全燃烧生成水蒸气,放出642kJ的热量:N2H4(l)+O2(g)═N2(g)+2H2O(g)△H=+642 kJ•mol-1 | |
| B. | 12 g石墨转化为CO时,放出110.5 kJ的热量:2C(石墨,s)+O2(g)═2CO(g)△H=-110.5 kJ•mol-1 | |
| C. | 已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-286 kJ•mol-1,则:2H2O(l)═2H2(g)+O2(g)的△H=+572 kJ•mol-1 | |
| D. | 已知N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ•mol-1,则在一定条件下向密闭容器中充入0.5 mol N2(g)和1.5 mol H2(g)充分反应放出46.2 kJ的热量 |
12.下列关于苯酚的叙述不正确的是( )
| A. | 苯酚是一种弱酸,滴加指示剂会变色 | |
| B. | 苯酚在水溶液中能按下式电离: | |
| C. | 苯酚钠水溶液里通入CO2气体总是生成NaHCO3 | |
| D. | 苯酚有腐蚀性,溅在皮肤上可用酒精冲洗 |