题目内容
下列有关化学用语表示正确的是( )
| A、中子数为8的N原子:78N |
B、离子结构示意图: 只能表示35Cl- 只能表示35Cl- |
| C、碳酸氢钠在水溶液中的电离方程式:NaHCO3=Na++HCO3- |
| D、作为相对原子质量标准的碳原子:614C |
考点:分子、原子、离子,电离方程式的书写
专题:
分析:A.质量数=质子数+中子数;
B.可表示质子数为17的氯离子;
C.碳酸氢钠为强电解质,完全电离,但碳酸氢根离子保留整体;
D.作为相对原子质量标准的碳原子为12-C原子.
B.可表示质子数为17的氯离子;
C.碳酸氢钠为强电解质,完全电离,但碳酸氢根离子保留整体;
D.作为相对原子质量标准的碳原子为12-C原子.
解答:
解:A.质量数=质子数+中子数=7+8=15,中子数为8的N原子:715N,故A错误;
B.离子结构示意图: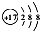 可表示35Cl-,或表示37Cl-,故B错误;
可表示35Cl-,或表示37Cl-,故B错误;
C.碳酸氢钠在水溶液中的电离方程式为NaHCO3═Na++HCO3-,故C正确;
D.作为相对原子质量标准的碳原子为126C,故D错误;
故选C.
B.离子结构示意图:
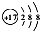 可表示35Cl-,或表示37Cl-,故B错误;
可表示35Cl-,或表示37Cl-,故B错误;C.碳酸氢钠在水溶液中的电离方程式为NaHCO3═Na++HCO3-,故C正确;
D.作为相对原子质量标准的碳原子为126C,故D错误;
故选C.
点评:本题考查化学用语,涉及离子结构示意图、电离方程式、原子的构成等,注重基础知识的考查,注意规范使用化学用语,题目难度不大.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
25℃时,水的电离达到平衡:H2O?H++OH-;△H>0,下列叙述正确的是( )
| A、向水中加入稀氨水,平衡逆向移动,KW减小 |
| B、向水中加入少量固体硫酸钠,平衡不移动,KW不变 |
| C、向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D、向水中加入少量固体NH4Cl,平衡正向移动,c(H+)降低 |
下列说法正确的是( )
| A、CO2的摩尔质量为44g |
| B、标准状况下,2.24L CCl4所含的原子数为0.5NA |
| C、5.4mL4℃的H2O中有1.806×1023个分子 |
| D、50mL 1mol/L BaCl2溶液中,Ba2+和Cl-物质的量之和是0.1mol |
足量的铝粉分别和等体积pH=12的氢氧化钠溶液以及pH=2的某酸溶液反应,放出氢气的体积分别为V1、V2,则在相同状况下,V1、V2的关系可能是( )
| A、V1<V2 |
| B、V1=3V2 |
| C、V1>V2 |
| D、以上三种情况都有可能 |