题目内容
10.下列事实不能用勒夏特列原理解释的是( )| A. | 溴水中当加入硝酸银溶液后,溶液颜色变浅 | |
| B. | 高压比常压有利于工业合成氨反应 | |
| C. | 红棕色NO2加压后颜色比原来要深 | |
| D. | 热的纯碱除油污效果好 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动,使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答 解:A.溴水中有下列平衡:Br2+H2O?HBr+HBrO,加入硝酸银溶液后,会和HBr反应生成AgBr沉淀,所以平衡正向移动,溶液颜色变浅,能用勒夏特列原理解释,故A不选;
B.合成氨的正反应是一个反应前后气体体积减小的可逆反应,增大压强平衡正向移动,所以高压比常压有利于工业合成氨反应,可以用勒夏特里原理解释,故B不选;
C.对2NO2?N2O4平衡体系增加压强,平衡正向移动,颜色变浅,但变浅后的颜色仍然比原来颜色深,不能用勒夏特列原理解释,故C选;
D.升高温度促进纯碱水解导致溶液碱性增强,则除油污效果更好,可以用勒夏特列原理解释,故D故选;
故选C.
点评 本题考查了化学平衡移动原理的分析判断,为高频考点,侧重于学生的分析能力的考查,影响因素的分析,平衡移动原理的理解是解题关键,易错选项是C.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
8.有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
为了鉴别上述化合物.分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀完全溶解;
③进行焰色反应,B、C为紫色(透过蓝色钴玻璃),A、E为黄色;
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀,B中无明显现象.
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、C的化学式:BKNO3;CKAl(SO4)2.
(2)写出过量E滴入到C溶液中的离子反应方程式Al3++4OH-═AlO2-+2H2O.
(3)在A溶液中加澄清石灰水,其离子方程式为HCO3-+Ca2++OH-=CaCO3↓+H2O.
(4)写出检验D中阴离子的方法取样,先加盐酸,再滴加氯化钡溶液.
| 阳离子 | K+、Na+、Al3+、Cu2+ |
| 阴离子 | OH-、HCO3-、NO3-、SO42- |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀完全溶解;
③进行焰色反应,B、C为紫色(透过蓝色钴玻璃),A、E为黄色;
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀,B中无明显现象.
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、C的化学式:BKNO3;CKAl(SO4)2.
(2)写出过量E滴入到C溶液中的离子反应方程式Al3++4OH-═AlO2-+2H2O.
(3)在A溶液中加澄清石灰水,其离子方程式为HCO3-+Ca2++OH-=CaCO3↓+H2O.
(4)写出检验D中阴离子的方法取样,先加盐酸,再滴加氯化钡溶液.
5.下列离子方程式正确的是( )
| A. | 氯气通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 向Fe(OH)3中加入氢溴酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 向Fe(NO3)2稀溶液中加入盐酸:Fe2++4H++NO3-═Fe3++NO↑+2H2O | |
| D. | 向NaHCO3溶液中加入过量的Ba(OH)2溶液:Ba2++2HCO3-+2OH-═BaCO3↓+CO32-+2H2O |
15.下列物质的类别与所含官能团都正确的是( )
| A. | 醇类-OH | B. | 羧酸-CHO | C. | 酯类-CHO | D. | 醚类 CH3-O-CH3 |
2.钛被誉为“21世纪金属”,具有多种优良性能,工业上冶炼金属钛的反应原理为4Na+TiCl4$\frac{\underline{\;高温\;}}{\;}$Ti+4NaCl.下列说法正确的是( )
| A. | TiCl4是还原剂 | B. | Na被氧化 | ||
| C. | Na得到电子 | D. | TiCl4发生氧化反应 |
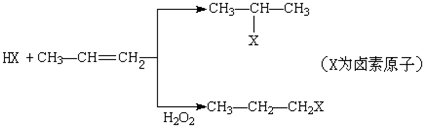
 的物质,该物质是一种香料.
的物质,该物质是一种香料.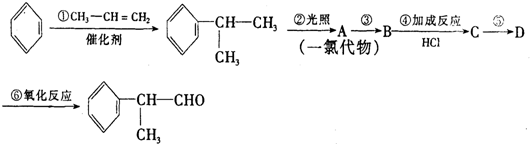
 ,
,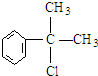 .
.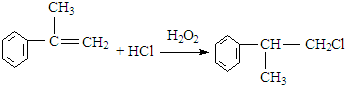 .反应⑤的化学方程式为(有机物写结构简式,并注明反应条件):
.反应⑤的化学方程式为(有机物写结构简式,并注明反应条件):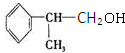 +NaCl.
+NaCl.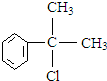 的水解产物
的水解产物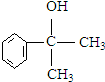 不能经氧化反应⑥而得到产品,导致产率低.
不能经氧化反应⑥而得到产品,导致产率低. ,
, ,
, .
.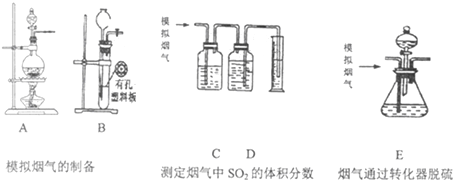
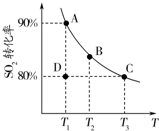 研究硫及其化合物性质有重要意义.
研究硫及其化合物性质有重要意义.