题目内容
8.实验室用98%的浓硫酸(密度为1.84g/mL)配置100mL 1mol/L的稀硫酸,已选用的主要仪器有烧杯、胶头滴管、玻璃棒,还缺少的仪器是( )| A. | 容量瓶、10mL量筒 | B. | 容量瓶、100mL量筒 | ||
| C. | 100mL容量瓶、50mL量筒 | D. | 100mL容量瓶、10mL量筒 |
分析 操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,根据配制一定物质的量浓度的溶液的操作步骤选择仪器,以此解答该题.
解答 解:该浓硫酸的物质的量浓度为:c=$\frac{1000ρω}{M}$=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,
配制100mL 1mol/L的稀硫酸,需要浓硫酸的体积为:$\frac{0.1L×1mol/L}{18.4mol/L}$≈0.0136L=0.0054mL,应该选用10mL量筒;
配制100mL 1mol/L的稀硫酸,应该选用100mL容量瓶,
故选D.
点评 本题考查配制一定物质的量浓度的溶液中选用仪器的方法,为高频考点,侧重考查学生的分析能力和实验能力,题目难度中等,注意掌握物质的量浓度与溶质质量分数之间的转化,明确配制一定物质的量浓度的溶液方法及选用仪器规格的原则.

练习册系列答案
相关题目
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L HF中含有的电子数为10NA | |
| B. | 在一定条件下,1molSO2和0.5molO2在密闭容器中充分反应,转移电子数目为2NA | |
| C. | 常温常压下,32gN2H4中含有的共价键数目为5NA | |
| D. | 某饱和FeCl3溶液中,若Fe3+的数目为NA,则Cl-的数目为3NA |
20. 生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:下列有关说法不正确的是( )
生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:下列有关说法不正确的是( )
 生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:下列有关说法不正确的是( )
生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:下列有关说法不正确的是( )| A. | NaHCO3溶液的物质的量浓度为0.8 mol/L | |
| B. | b点与c点溶液所含微粒种类相同 | |
| C. | a点溶液中存在的离子是Na+、AlO2-、OH-、H+ | |
| D. | 生成沉淀的离子方程式为:HCO3-+AlO2-+H2O═Al(OH)3↓+CO32- |
17.我国的纳米基础研究能力已跻身于世界前列,例知曾制得一种合成纳米材料,其化学式为RN.己知该化合物中的Rn-核外有28个电子,则R元素位于元素周期表的( )
| A. | 第三周期第ⅤA族 | B. | 第四周期第ⅤA族 | C. | 第五周期第ⅢA族 | D. | 第四周期第ⅢA族 |
1.将1.52g铜镁合金完全溶解于50mL密度为1.40g•mL-1、质量分数为63%的浓硝酸得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol•L-1NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A. | 该合金中铜与镁的物质的量之比是2:1 | |
| B. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol•L-1 | |
| C. | 得到2.54g沉淀时,加入NaOH溶液的体积是600L | |
| D. | NO2和N2O4的混合气体中,NO2的体积分数是80% |
 用胆矾晶体(CuSO4•5H2O )配制0.40mol/L的CuSO4溶液240mL,回答下列问题
用胆矾晶体(CuSO4•5H2O )配制0.40mol/L的CuSO4溶液240mL,回答下列问题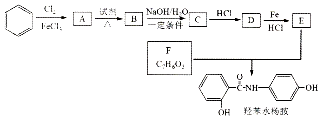
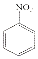 $→_{HCl}^{Fe}$
$→_{HCl}^{Fe}$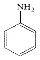
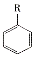 (R-烷基)$\stackrel{KMnO_{4}/H+}{→}$
(R-烷基)$\stackrel{KMnO_{4}/H+}{→}$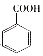
 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$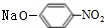 +NaCl+H2O.
+NaCl+H2O.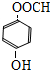 .
.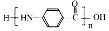 的合成路线
的合成路线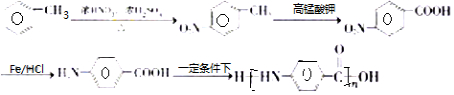 .
.