题目内容
把煤作为燃料可以通过下列两种途径:途径Ⅰ:C(s)+O2(g)![]() CO2(g)(放热Q1 kJ)
CO2(g)(放热Q1 kJ)
途径Ⅱ:先制水煤气:
C(s)+H2O(g)![]() CO(g)+H2(g)(吸热Q2 kJ)
CO(g)+H2(g)(吸热Q2 kJ)
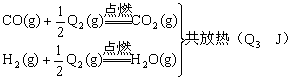
再燃烧水煤气:

试完成下列问题:
(1)判断两种途径放热:途径Ⅰ放出的热量____________(填“大于”“等于”或“小于”)途径Ⅱ放出的热量。
(2)Q1、Q2、Q3的数学关系式是____________。
(3)由于制取水煤气反应里,反应物所具有的总能量____________生成物所具有的总能量,那么在化学反应时,反应物应需要____________能量才能转化为生成物,因此其反应条件为____________。
(4)简述煤通过途径Ⅱ作为燃料的意义。
_____________________________________________________________________。
解析:由盖斯定律知,只要初态和末态相同,不管反应分几个过程,吸、放热均相同。
答案:(1)等于
(2)Q1=Q2+Q3
(3)小于 吸收 高温
(4)燃烧更充分,清洁无污染。

练习册系列答案
相关题目
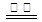 CO2(g) ΔH=E1 ①
CO2(g) ΔH=E1 ① _____(填“大于”、“等于”、“小于”)途径II放出的热量。
_____(填“大于”、“等于”、“小于”)途径II放出的热量。 是_____________________________________。
是_____________________________________。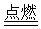 CO2(g) ΔH=Q1kJ
CO2(g) ΔH=Q1kJ O2(g)
O2(g)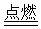 CO2(g) ΔH=Q3kJ
CO2(g) ΔH=Q3kJ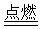 H2O(g) ΔH=Q4kJ
H2O(g) ΔH=Q4kJ