题目内容
2.下列实验“操作和现象”与“结论”都正确的是( )| 选项 | 操作和现象 | 结论 |
| A | 向溶液中加入KSCN溶液无明显现象,再加入新制氯水,溶液呈血红色 | 证明原溶液中含有Fe2+ |
| B | 加入AgNO3溶液后生成白色沉淀,加稀盐酸沉淀不溶解 | 可确定有Cl-存在 |
| C | 将某种气体通入酸性KMnO4溶液.溶液褪色 | 说明该气体一定具有漂白性 |
| D | 向某溶液中逐渐通入CO2气体,先出现白色胶状沉淀,继续通入CO2气体,白色胶状沉淀不溶解 | 证明该溶液中存在AlO2- |
| A. | A | B. | B | C. | C | D. | D |
分析 A.向溶液中加入KSCN溶液无明显现象,说明溶液中不存在铁离子,再加入新制氯水,溶液呈血红色,说明原溶液中含有亚铁离子;
B.应该用稀硝酸具有银离子,稀盐酸中含有氯离子,不能使用稀盐酸;
C.酸性高锰酸钾溶液具有强氧化性,则褪色原因可能是通入的气体具有还原性,如乙烯、乙炔等;
D.原溶液中可能会有硅酸根离子,不一定含有偏铝酸根离子.
解答 解:A.向溶液中加入KSCN溶液无明显现象,排除了铁离子的干扰,然后再加入新制氯水,溶液呈血红色,说明此时溶液中存在铁离子,从而说明原溶液中存在亚铁离子,故A正确;
B.加入AgNO3溶液后生成白色沉淀,然后加入稀硝酸后白色沉淀不溶解,从而证明原溶液中含有Cl-,而不能用稀盐酸酸化,故B错误;
C.将某种气体通入酸性KMnO4溶液.溶液褪色,通入的气体可能为乙炔、乙烯等具有还原性的气体,不一定具有漂白性,故C错误;
D.向某溶液中逐渐通入CO2气体,先出现白色胶状沉淀,继续通入CO2气体,白色胶状沉淀不溶解,生成的沉淀可能为硅酸,不一定为氢氧化铝,则原溶液中不一定含有偏铝酸根离子,故D错误;
故选A.
点评 本题考查了实验方案的设计与评价,题目难度中等,明确常见物质组成、性质及检验方法为解答关键,B为易错点,注意检验氯离子时不能用稀盐酸酸化,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.物质的量浓度相同的硫酸铝钾[KA1(S04)2]和Ba(0H)2两种溶液按1:2的体积比混合,下列分析中正确的是( )
| A. | 得到沉淀的物质的量最大 | B. | 得到沉淀的质量最大 | ||
| C. | 反应后溶液仍含有Al3+ | D. | 反应后溶液仍含有AlO2- |
10.下列说法正确的是( )
| A. | 在25℃、1.01×105Pa的条件下,2.24 L H2中含有的分子数小于0.1NA | |
| B. | 1 L 1 mol•L-1的CaCl2溶液中含Cl-的数目为NA | |
| C. | 在标准状况下,22.4 L H2O的质量约为18 g | |
| D. | 22 g CO2与标准状况下11.2 L H2O含有相同的分子数 |
17.现有常温下pH=2的盐酸甲和pH=2的醋酸溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol•L-1的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+)B.c(H+)/c(CH3COOH)
C.c(H+)•c(OH-)D.c(OH-)/c(H+)
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡向右(填“向左”“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的值将减小(填“增大”“减小”或“无法确定”).
(3)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为pH(甲)>pH(乙)(填“>”“<”或“=”).
(4)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为V(甲)<V(乙)(填“>”“<”或“=”).
(5)已知25℃时,两种酸的电离平衡常数如下:
下列四种离子结合H+能力最强的是B.
A.HCO3- B.CO32- C.ClO-D.CH3COO-
写出下列反应的离子方程式:
CH3COOH+Na2CO3(少量):2CH3COOH+CO32-=H2O+2CH3COO-+CO2↑;
HClO+Na2CO3(少量):HClO+CO32-=ClO-+HCO3-.
(1)常温下0.1mol•L-1的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+)B.c(H+)/c(CH3COOH)
C.c(H+)•c(OH-)D.c(OH-)/c(H+)
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡向右(填“向左”“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的值将减小(填“增大”“减小”或“无法确定”).
(3)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为pH(甲)>pH(乙)(填“>”“<”或“=”).
(4)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为V(甲)<V(乙)(填“>”“<”或“=”).
(5)已知25℃时,两种酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡 常数 | K1 | 1.8×10-5 | 4.2×10-7 | 3.0×10-8 |
| K2 | 5.6×10-11 | -- | ||
A.HCO3- B.CO32- C.ClO-D.CH3COO-
写出下列反应的离子方程式:
CH3COOH+Na2CO3(少量):2CH3COOH+CO32-=H2O+2CH3COO-+CO2↑;
HClO+Na2CO3(少量):HClO+CO32-=ClO-+HCO3-.
14.某无色透明的酸性溶液能与铁反应生成氢气,则该溶液中一定能够大量共存的是( )
| A. | NH4+、K+、Ca2+、Cl- | B. | SO42-、Na+、Fe2+、Cl- | ||
| C. | Na+、K+、Cl-、SiO32- | D. | SO42-、NO3-、K+、Na+ |
11.下列有关操作正确的是( )
| A. | 将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,实现乙醇被氧化为乙醛的实验 | |
| B. | 相对分子质量相同的不同物质一定是同分异构体 | |
| C. | 淀粉和纤维素的分子式相同,所以两者互为同分异构体 | |
| D. | 可以用水鉴别硝基苯、乙醇、四氯化碳三种有机物 |
12.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构.则下列叙述正确的是( )
| A. | 原子半径 A>B>D>C | B. | 原子序数d>c>b>a | ||
| C. | 离子半径 C>D>B>A | D. | 还原性 B>A>D>C |
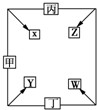 甲、乙、丙、丁四种单质在点燃条件下反应生成X、Y、Z、W四种化合物,其转化关系如图所示.又如:
甲、乙、丙、丁四种单质在点燃条件下反应生成X、Y、Z、W四种化合物,其转化关系如图所示.又如: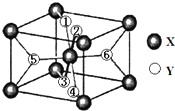 在元素周期表中,除稀有气体外几乎所有元素都能与氢形成氢化物.氢化物晶体的结构有共价型和离子型之分.
在元素周期表中,除稀有气体外几乎所有元素都能与氢形成氢化物.氢化物晶体的结构有共价型和离子型之分.