题目内容
现有下列物质:①硫酸钡;②明矾;③浓硫酸;④蒸馏水;⑤SO3;⑥醋酸铵.其中属于强电解质的有 ,属于弱电解质的有 ,属于非电解质的有 .写出醋酸铵在水中的电离方程式 .
考点:强电解质和弱电解质的概念,电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:能全部电离的电解质是强电解质;只有部分电离的电解质是弱电解质;在水溶液里或熔融状态下都不导电的化合物是非电解质;据这些概念解答即可.
解答:
解:能全部电离的电解质是强电解质,硫酸钡、明矾醋酸铵在水溶液里能全部电离,所以都是强电解质,故答案为:①、②、⑥;
只有部分电离的电解质是弱电解质,蒸馏水只有部分电离,所以是弱电解质,故答案为:④;
在水溶液里或熔融状态下都不导电的化合物是非电解质,三氧化硫是非电解质,故答案为:⑤;
醋酸铵属于盐,是强电解质,电离方程式为:CH3COONH4=CH3COO-+NH4+,故答案为:CH3COONH4=CH3COO-+NH4+.
只有部分电离的电解质是弱电解质,蒸馏水只有部分电离,所以是弱电解质,故答案为:④;
在水溶液里或熔融状态下都不导电的化合物是非电解质,三氧化硫是非电解质,故答案为:⑤;
醋酸铵属于盐,是强电解质,电离方程式为:CH3COONH4=CH3COO-+NH4+,故答案为:CH3COONH4=CH3COO-+NH4+.
点评:本题考查了电解质、非电解质、强电解质和弱电解质的判断,难度不大,根据定义判断即可.

练习册系列答案
相关题目
装置如图:关闭装置A中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示;关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶.则关于A、B两装置是否漏气的有关说法正确的是( )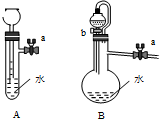

| A、A装置肯定不漏气,B装置肯定漏气 |
| B、A装置肯定漏气,B装置可能不漏气 |
| C、A装置肯定不漏气,B装置肯定不漏气 |
| D、A装置肯定不漏气,B装置可能漏气也可能不漏气 |
下列化学元素中属于组成生物体的微量元素的是( )
| A、K | B、P | C、B | D、Ca |
将0.1mol?L-1CH3COOH溶液加水稀释或加入少量的CH3COONa晶体时,都会引起( )
| A、溶液的pH增大 |
| B、溶液中的c(H+)增大 |
| C、溶液的导电能力减弱 |
| D、溶液中的c(OH-)减小 |
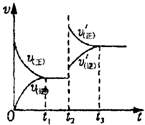 一定温度下,某容积恒定的密闭容器中发生如下可逆反应:CO(g)+H2(g)?C(s)+H2O(g);△H<0以l mol CO和2mol H2为起始反应物,tl时达到平衡,生成0.6mol H2O(g).t2时改变反应条件,化学反应速率(v)与时间(t)的关系如图所示.下列叙述正确的是( )
一定温度下,某容积恒定的密闭容器中发生如下可逆反应:CO(g)+H2(g)?C(s)+H2O(g);△H<0以l mol CO和2mol H2为起始反应物,tl时达到平衡,生成0.6mol H2O(g).t2时改变反应条件,化学反应速率(v)与时间(t)的关系如图所示.下列叙述正确的是( )| A、起始时刻和t1达到平衡后气体的物质的量之比为4:5 |
| B、平衡后若加入少量碳,平衡向逆反应方向移动 |
| C、平衡后若加入氢气,上述反应的△H会增大 |
| D、t2时改变的条件可能是增大了压强 |