题目内容
卤族元素单质具有相似的化学性质,这主要是由于卤素( )
| A、单质均为双原子分子 |
| B、均为非金属元素 |
| C、原子最外层电子数相同,均为7个 |
| D、原子核外电子层数依次增大 |
考点:氯、溴、碘及其化合物的综合应用
专题:
分析:同一主族元素,原子最外层电子数相等,元素的性质取决于最外层电子数,所以同一主族元素性质具有相似性,据此分析解答.
解答:
解:卤族元素原子最外层都有7个电子,在化学所以中易得电子而体现氧化性,所以其单质的化学性质相似,与分子构成、元素是否是非金属元素、原子核外电子层数都无关,故选C.
点评:本题考查卤族元素性质相似的原因,结构决定性质,性质体现结构,明确元素性质及原子最外层电子之间的关系即可解答,题目难度不大.

练习册系列答案
相关题目
实验室中欲制氢气,最好的方法是( )
| A、纯锌与稀硫酸反应 |
| B、纯锌与浓硫酸反应 |
| C、粗锌(含铅.铜杂质)与浓硝酸反应 |
| D、粗锌(含铅.铜杂质)与稀硫酸反应 |
铜和镁的合金4.6g完全溶于浓硝酸,若反应后硝酸被还原只产生 2.24L的 NO2气体和1.12L的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为( )
| A、9.02g |
| B、8.51g |
| C、8.00g |
| D、7.04g |
钢铁制品表面镀铝既美观又能防腐.镀铝时选用的阳极材料是( )
| A、Zn |
| B、Fe |
| C、Al |
| D、AlCl3 |
X、Y两元素可形成X2Y3型化合物,则X、Y原子基态时最外层的电子排布可能是( )
| A、X:3s23p1 Y:3s23p5 |
| B、X:2s22p3 Y:2s22p5 |
| C、X:3s23p1 Y:3s23p4 |
| D、X:3s2 Y:2s22p3 |
能源可划分为一级能源和二级能源.自然界中以现成形式提供的能源称为一级能源,需依靠其它能源的能量间接制取的能源成为二级能源.下列能源是一级能源的是( )
| A、电能 | B、太阳能 |
| C、氢气 | D、水煤气 |
某溶液中只含Na+、Mg2+、SO42-、Cl-,其物质的量浓度比为Na+:Mg2+:Cl-=3:5:5,若Na+的浓度为3mol/L,则SO42-的浓度为( )
| A、2 mol/L |
| B、3 mol/L |
| C、4 mol/L |
| D、8 mol/L |
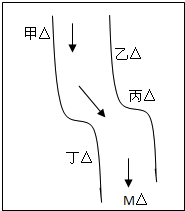 在一条鱼、虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如图所示),它们排出的废液里,每个工厂只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水检测时发现:①甲处河水呈乳白色,②乙处河水呈红褐色,③丙处河水由浑变清,④丁处产生气泡,河水仍清,⑤M处水样的pH小于7.请判断:
在一条鱼、虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如图所示),它们排出的废液里,每个工厂只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水检测时发现:①甲处河水呈乳白色,②乙处河水呈红褐色,③丙处河水由浑变清,④丁处产生气泡,河水仍清,⑤M处水样的pH小于7.请判断: