题目内容
14.下列说法正确的是( )| A. | 离子晶体中只含有离子键,不含有共价键 | |
| B. | 水分子很稳定,因为水分子间存在氢键 | |
| C. | 分子晶体中一定存在分子间作用力,不一定存在共价键 | |
| D. | I的原子半径大于Br,HI比HBr的热稳定性强 |
分析 A.离子晶体一定含有离子键,可能含有共价键;
B.分子的稳定性与共价键有关;
C.分子晶体中分子间存在分子间作用力,分子内可能存在共价键;
D.同主族从上到下原子半径逐渐增大,非金属性逐渐减弱.
解答 解:A.离子晶体一定含有离子键,可能含有共价键,如NaOH存在O-H键,为共价键,故A错误;
B.稳定性属于化学性质,而分子间作用力影响物理性质,分子的稳定性与共价键有关,与氢键无关,故B错误;
C.分子晶体中分子间存在分子间作用力,分子内可能存在共价键,如为单原子分子,则不存在共价键,故C正确;
D.同主族从上到下原子半径逐渐增大,非金属性逐渐减弱,对应的氢化物的稳定性减弱,故D错误.
故选C.
点评 本题考查较为综合,涉及化学键、晶体类型以及元素周期率的递变等知识,为高考常见题型,侧重于原子结构与元素周期率的考查,注意把握共价键、离子键的区别,把握元素周期率的递变规律,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列有关物质的分离或提纯的说法中正确的是( )
| A. | 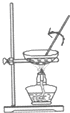 图:从FeCl2溶液中制取FeCl2晶体 | |
| B. | 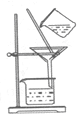 图:从制取Fe(OH)2胶体的混合物中提纯胶体 | |
| C. | 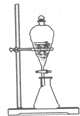 图:用CCl4萃取,从溴水中得到纯溴 | |
| D. | 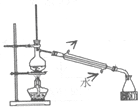 图:分离苯和甲苯 |
5.下列说法不正确的是( )
| A. | 用洁净铂丝蘸取未知溶液进行焰色反应,呈黄色火焰,则该溶液有Na+,但不能确定K+的存在 | |
| B. | 实验室制取乙酸乙酯时,向试管中加入乙醇,然后边摇动试管边慢慢加入浓硫酸和冰醋酸 | |
| C. | 用已知浓度NaOH溶液滴定未知浓度盐酸,滴定终点时,俯视刻度线,则测得盐酸浓度偏小 | |
| D. | 相同温度下,可以通过观察气泡多少来比较不同浓度Na2SO3溶液与稀H2SO4溶液反应的快慢 |
2.透明强酸性溶液中,下列各组离子一定能大量共存的是( )
| A. | Cl-、Cu2+、SO42-、NO3- | B. | Cl-、Na+、SO42-、CH3COO- | ||
| C. | Cl-、Fe2+、MnO4-、NO3- | D. | AlO2-、Na+、SO42-、NO3- |
9.下列物质中碳元素含量最高的是( )
| A. | 甲烷 | B. | 乙烷 | C. | 乙烯 | D. | 苯 |
3.下列说法中,正确的是( )
| A. | 1 mol氢约含有阿伏伽德罗常数个氢 | |
| B. | 1 molCaCl2含有2 mol Cl- | |
| C. | 1 mol氢气含有6.02×1023个电子 | |
| D. | 1 molH2O含有1 molH2和1 molO |
17.某溶液加入金属铝能放出氢气.下列各组离子在该溶液中一定可以大量共存的是( )
| A. | Fe3+、H+、Cl- SO42- | B. | Na+、K+、Ba2+、HCO3- | ||
| C. | Na+ Cl- NO3- K+ | D. | K+ Na+ Cl- SO42- |

 .
.