题目内容
下列说法正确的是( )
| A、0.5 mol Fe2+与含0.5 mol H2O2溶液反应,转移NA个电子(NA表示阿伏加德罗常数) | ||
B、常温时,0.1mol/L HA溶液的pH>1,0.1mol/L BOH溶液中
| ||
| C、复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是2 Fe3++3SO42-+3Ba2++6 OH-=3BaSO4↓+2Fe(OH)3↓ | ||
| D、向2mL 0.1mol/L的硝酸银溶液中滴加几滴0.1mol/L氯化钠溶液,产生白色沉淀,再滴加几滴硫化钠溶液,产生黑色沉淀,说明氯化银能转化为更难溶的硫化银 |
考点:离子浓度大小的比较,离子方程式的书写,氧化还原反应的电子转移数目计算,难溶电解质的溶解平衡及沉淀转化的本质
专题:基本概念与基本理论
分析:A.Fe2+与H2O2反应离子方程式为:2H++2Fe2++H2O2=2H2O+2Fe3+,根据亚铁离子的物质的量进行计算;
B.0.1mol/L HA溶液的pH>1,则HA是弱酸,0.1mol/L BOH溶液中
=1012,c(OH-).c(H+)=10-14,所以c(OH-)=0.1mol/L,则BOH为强碱,二者等物质的量混合时恰好反应生成BA,BA为强碱弱酸盐,其溶液呈碱性,再结合电荷守恒判断;
C.复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液时,SO42- 和Ba2+生成BaSO4沉淀,Fe3+和 OH-反应生成沉淀,当Fe3+完全反应后,铵根离子和 OH-反应生成一水合氨;
D.硫离子和银离子反应生成硫化银黑色沉淀.
B.0.1mol/L HA溶液的pH>1,则HA是弱酸,0.1mol/L BOH溶液中
| c(OH-) |
| c(H+) |
C.复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液时,SO42- 和Ba2+生成BaSO4沉淀,Fe3+和 OH-反应生成沉淀,当Fe3+完全反应后,铵根离子和 OH-反应生成一水合氨;
D.硫离子和银离子反应生成硫化银黑色沉淀.
解答:
解:A.Fe2+与H2O2反应离子方程式为:2H++2Fe2++H2O2=2H2O+2Fe3+,根据方程式知,亚铁离子和双氧水以1:1反应,所以要根据亚铁离子计算转移电子数,转移电子数=0.5mol×(3-2)×NA/mol=0.5NA,故A错误;
B.0.1mol/L HA溶液的pH>1,则HA是弱酸,0.1mol/L BOH溶液中
=1012,c(OH-).c(H+)=10-14,所以c(OH-)=0.1mol/L,则BOH为强碱,二者等物质的量混合时恰好反应生成BA,BA为强碱弱酸盐,其溶液呈碱性c(OH-)>c(H+),再结合电荷守恒得c(B+)>c(A-),盐类水解较微弱,所以c(OH-)<c(A-),故C错误;
C.复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液时,SO42- 和Ba2+生成BaSO4沉淀,Fe3+和 OH-反应生成沉淀,当Fe3+完全反应后,铵根离子和 OH-反应生成一水合氨,所以当滴加少量氢氧化钡溶液时,可能发生反应2 Fe3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Fe(OH)3↓,故C正确;
D.硝酸银溶液中滴加少量氯化钠溶液,则溶液中还存在自由移动的银离子,再加硫化钠时,硫化钠直接和银离子反应生成黑色的硫化银沉淀,而不是由氯化银转化为硫化银,故D错误;
故选C.
B.0.1mol/L HA溶液的pH>1,则HA是弱酸,0.1mol/L BOH溶液中
| c(OH-) |
| c(H+) |
C.复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液时,SO42- 和Ba2+生成BaSO4沉淀,Fe3+和 OH-反应生成沉淀,当Fe3+完全反应后,铵根离子和 OH-反应生成一水合氨,所以当滴加少量氢氧化钡溶液时,可能发生反应2 Fe3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Fe(OH)3↓,故C正确;
D.硝酸银溶液中滴加少量氯化钠溶液,则溶液中还存在自由移动的银离子,再加硫化钠时,硫化钠直接和银离子反应生成黑色的硫化银沉淀,而不是由氯化银转化为硫化银,故D错误;
故选C.
点评:本题考查较综合,涉及离子反应先后顺序、难溶物的转化、氧化还原反应等知识点,A选项要确定过量计算、B选项要确定碱的强弱、C选项要考虑离子反应先后顺序,这些知识点都是易错点,解题时要注意,难度中等.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
下列实验能达到目的是( )
A、 用酒精萃取溴水中的溴 |
B、 将硫酸铜溶液直接蒸干得到胆矾 |
C、 说明2NO2(g)?N2O4(g)△H<0 |
D、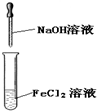 实验室制备Fe(OH)2 |
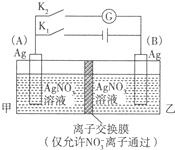 利用如图装置进行实验,甲乙两池均为1mol?L-1的AgNO3溶液,A、B均为Ag电极.实验开始先闭合K1,断开K2.一段时间后,断开K1,闭合K2,形成浓差电池,电流计指针偏转(Ag+浓度越大氧化性越强).下列说法不正确的是( )
利用如图装置进行实验,甲乙两池均为1mol?L-1的AgNO3溶液,A、B均为Ag电极.实验开始先闭合K1,断开K2.一段时间后,断开K1,闭合K2,形成浓差电池,电流计指针偏转(Ag+浓度越大氧化性越强).下列说法不正确的是( )| A、闭合K1,断开K2后,A电极增重 |
| B、闭合K1,断开K2后,乙池溶液浓度上升 |
| C、断开K1,闭合K2后,NO3-向B电极移动 |
| D、断开K1,闭合K2后,A电极发生氧化反应 |
在水溶液中能大量共存的一组离子是( )
| A、Al3+、Na+、HCO3-、SO42- |
| B、H+、Fe2+、ClO-、Cl- |
| C、Na+、Ag+、Cl-、SO42- |
| D、K+、Ba2+、NO3-、Cl- |
硼的原子序数为5,硼的最高价含氧酸的化学式不可能是( )
| A、HBO2 |
| B、H3BO3 |
| C、H2BO3 |
| D、H4B2O5 |
对100mL 1mol?L-1的Na2CO3溶液,下列说法不正确的是( )
A、将溶液稀释,
| ||
| B、滴入含0.1 mol CH3COOH的溶液:c(CH3COO-)<c(HCO3-) | ||
| C、通入0.1 mol CO2气体,溶液中存在:c(Na+)=c(CO32-)十c(HCO3-)+c(H2CO3) | ||
| D、滴入酚酞,微热,溶液颜色加深 |
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理.该法的工艺流程为:CrO42-
Cr2O72-
Cr3+
Cr(OH)3↓,其中第①步存在平衡:2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O,下列说法错误的是( )
| H+ | ||
|
| Fe2+ | ||
|
| OH- | ||
|
| A、在第①反应平衡体系中加入水,溶液中c(H+)增大 |
| B、溶液的pH值不变时,说明第①步反应达平衡状态 |
| C、第②步中,还原0.01mol Cr2O72-离子,需要0.06mol的FeSO4?7H2O |
| D、上述三步转化反应中,只有一个反应为氧化还原反应 |
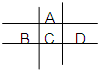 图为周期表的一小部分,A、B、C、D的位置关系如图所示.且它们均为短周期元素,其中C元素的最外层电子数是电子层数的2倍,回答下列问题:
图为周期表的一小部分,A、B、C、D的位置关系如图所示.且它们均为短周期元素,其中C元素的最外层电子数是电子层数的2倍,回答下列问题: