题目内容
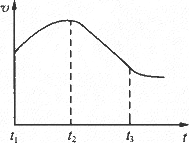
把除去氧化膜的镁条投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如图所示,其中t1~t2速率变化的主要原因是________,t2~t3速率变化的主要原因是________.
答案:
解析:
提示:
解析:
|
答案:因为反应放热,溶液温度升高,反应速率加快,因为随反应进行,盐酸的浓度减小较大,反应速度减慢 思路与技巧:这是一道训练发散性思维的习题,解答此题主要依据图示速率曲线的变化,对照影响化学反应速率的相关因素进行分析. 从图中可知速率曲线从t1时某一高度上升到t2后下降.这与盐酸的浓度随反应进行,t1→t2→t3逐渐减小,速率也应逐渐减小矛盾.然而事实就是这样.如何从影响反应速率的其他外界因素——压强、温度、催化剂角度去分析呢?从反应本质和反应外界条件来看,压强、催化剂(没加入催化剂)的影响均可排除.温度的影响是重点对象和关键.这就要看我们在做实验的时候,是否认真、细心观察所发生的一切现象,并有所感受.若从温度的影响来看肯定是升高了反应体系的温度,且温度升高的影响大于浓度减小的影响,但并没有加热,所以只能是反应本身所产生的热量所致.t2→t3主要是浓度减小占主要影响因素了. |
提示:
|
在实际实验过程中,往往有几个因素同时对速率产生作用,其中一个往往起主要作用,同时随着反应的进行量变引起质变,起主要作用的因素会转化成次要因素,另一因素会转化为主要因素,例如本题中,一开始反应放热导致的温度上升是反应速率加快的主要因素,但随着反应的进行,放热越来越少,浓度的降低称为主要影响速率的因素,因此反应速率随之下降.在解题时把握矛盾的主要方面是至关重要的. |

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
 (1)某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.①由图中所给数据进行分析,该反应的化学方程式为
(1)某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.①由图中所给数据进行分析,该反应的化学方程式为 2Z
2Z


