题目内容
α鸢尾酮香料的分子结构如图所示,下列说法中不正确的是( )


| A、α鸢尾酮可与某种酚互为同分异构体 |
| B、1 mol α鸢尾酮最多可与3 mol H2加成 |
| C、α鸢尾酮能发生银镜反应 |
D、α鸢尾酮经加氢→消去→加氢可转变为 |
考点:有机物的结构和性质,有机物分子中的官能团及其结构
专题:有机物的化学性质及推断
分析:α鸢尾酮中含C=C和C=O,不饱和度为3,结合烯烃、酮的性质来解答.
解答:
解:A.α鸢尾酮中含C=C和C=O,不饱和度为3,其同分异构体可含苯环和酚-OH,即α鸢尾酮可与某种酚互为同分异构体,故A正确;
B.C=C和C=O,均与氢气发生加成反应,则1 mol α鸢尾酮最多可与3 mol H2加成,故B正确;
C.不含-CHO,则不能发生银镜反应,故C错误;
D.C=C加成为饱和烃结构,C=O加成生成醇,消去转化为烯烃再与氢气加成转化为饱和烃结构,碳链骨架不变,则α鸢尾酮经加氢→消去→加氢可转变为 ,故D正确;
,故D正确;
故选C.
B.C=C和C=O,均与氢气发生加成反应,则1 mol α鸢尾酮最多可与3 mol H2加成,故B正确;
C.不含-CHO,则不能发生银镜反应,故C错误;
D.C=C加成为饱和烃结构,C=O加成生成醇,消去转化为烯烃再与氢气加成转化为饱和烃结构,碳链骨架不变,则α鸢尾酮经加氢→消去→加氢可转变为
 ,故D正确;
,故D正确;故选C.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、酮、醛性质的考查,选项A为解答的难点,题目难度不大.

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
在A+B(s)?C反应中,若增大压强或降低温度,B的转化率均增大,则正确的是( )
| A、A是固体,C是气体,正反应吸热 |
| B、A是气体,C是固体或液体,正反应放热 |
| C、A是气体,C是气体,正反应放热 |
| D、A是气体,C是气体,正反应吸热 |
已知短周期元素的离子:aA3+、bB2+、cC2-、dD-具有相同的电子层结构,下列关系错误的是( )
| A、质子数:b>C |
| B、原子半径:r(A)>r(D) |
| C、离子的还原性:C2->D- |
| D、离子半径:r(B2+)>r(C2-) |
反应3Fe(S)+4H2O(g)=Fe3O4(s)+4H2(g),在一可变的容积的密闭容器中进行,下列说法正确的是( )
| A、增加Fe的量,其正反应速率增大 |
| B、将容器的体积缩小一半,其正反应速率增大,逆反应速率减小 |
| C、保持体积不变,充入水蒸气使体系压强增大,其正反应速率增大,逆反应速率减小 |
| D、保持压强不变,充入N2使容器的体积增大,其正反应速率减小,逆反应速率也减小 |
下列有关热化学方程式的叙述不正确的是( )
| A、已知2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ?mol-1,则氢气的燃烧热为285.8 kJ?mol-1 | ||||
| B、已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | ||||
C、500℃、30MPa下,将0.5mol N2和足量H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)
| ||||
| D、已知2C(s)+2O2(g)═2CO2(g)△H1 2C(s)+O2(g)═2CO(g)△H2,则△H1<△H2 |
已知A2+、B+、C-、D2-四种离子具有相同的电子排布结构,下列说法中正确的是( )
| A、这四种元素处于同一周期 |
| B、离子半径:A2+>B+>C->D2- |
| C、A与D的质子数相差4 |
| D、还原性:C-<D2- |
下列事实不能用勒夏特列原理解释的是( )
| A、红棕色NO2加压后颜色先变深后变浅 |
| B、实验室中常用排饱和食盐水的方法收集氯气 |
| C、SO2催化氧化成SO3的反应,使用过量的空气以提高二氧化硫的利用率 |
| D、压缩H2与I2(g)反应的平衡混合气体,颜色变深 |
有机物的化学性质主要由其官能团决定.苹果酸是一种有机酸,结构简式为: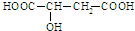 .下列有关苹果酸的说法不正确的是( )
.下列有关苹果酸的说法不正确的是( )
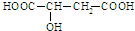 .下列有关苹果酸的说法不正确的是( )
.下列有关苹果酸的说法不正确的是( )| A、1mol苹果酸足量金属钠反应,生成氢气3g |
| B、1mol苹果酸与足量氢氧化钠溶液反应,消耗3mol氢氧化钠 |
| C、1mol苹果酸能与足量的碳酸氢钠溶液反应,标况下生成44.8L的二氧化碳气体 |
| D、苹果酸在一定条件下既能与醋酸反应,又能与乙醇反应,也可以自身发生酯化反应 |